Превенар 20
Лекарственная форма
суспензия для внутримышечного введения
Листок-вкладыш — информация для пациента
Превенар 20,
0,5 мл, суспензия для внутримышечного введения
▼ Лекарственный препарат подлежит дополнительному мониторингу, который способствует быстрому выявлению новых сведений о безопасности. Вы можете помочь, сообщая информацию о любых нежелательных реакциях, которые возникли в период применения лекарственного препарата (в том числе и о случаях его неэффективности). Способ сообщения о нежелательных реакциях описан в разделе 4 листка-вкладыша.
Перед применением препарата полностью прочитайте листок-вкладыш, поскольку в нём содержатся важные для Вас сведения.
Сохраните листок-вкладыш. Возможно, Вам потребуется прочитать его ещё раз.
Если у Вас возникли дополнительные вопросы, обратитесь к лечащему врачу.
Препарат назначен именно Вам. Не передавайте его другим людям. Он может навредить им, даже если симптомы их заболевания совпадают с Вашими.
Если у Вас возникли какие-либо нежелательные реакции, обратитесь к лечащему врачу. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в разделе 4 листка-вкладыша.
Содержание листка-вкладыша
- Что из себя представляет препарат Превенар 20, и для чего его применяют.
- О чём следует знать перед применением препарата Превенар 20.
- Применение препарата Превенар 20.
- Возможные нежелательные реакции.
- Хранение препарата Превенар 20.
- Содержимое упаковки и прочие сведения.
1. Что из себя представляет препарат Превенар 20, и для чего его применяют
Превенар 20 в качестве действующих веществ содержит пневмококковые конъюгаты полисахаридов двадцати серотипов, и обеспечивает защиту от 20 серотипов бактерий Streptococcus pneumoniae. Препарат относится к группе препаратов под названием «вакцины, пневмококковые вакцины».
Показания к применению
- у детей в возрасте от 6 недель до 18 лет, чтобы помочь предотвратить такие заболевания, как менингит (воспалительное поражение мозговых оболочек), сепсис или бактериемия (общий инфекционный процесс в следствие проникновения и циркуляции в крови бактерии), пневмония (воспаление лёгких) и отитов — (воспаление среднего уха), вызванные 20 серотипами бактерий Streptococcus pneumoniae;
- у взрослых в возрасте 18 лет и старше для профилактики таких заболеваний, как пневмония (воспаление лёгких), сепсис или бактериемия (общий инфекционный процесс вследствие проникновения и циркуляции в крови бактерии) и менингит (воспалительное поражение мозговых оболочек), вызванных 20 серотипами бактерии Streptococcus pneumoniae.
Способ действия препарата Превенар 20
Препарат действует, помогая организму вырабатывать собственные антитела, которые защищают Вас или Вашего ребёнка от этих заболеваний.
2. О чём следует знать перед применением препарата Превенар 20
Противопоказания
Не применяйте препарат Превенар 20:
- если у Вас или Вашего ребёнка тяжёлая аллергия на действующие вещества или любые другие компоненты препарата (перечисленные в разделе 6 листка-вкладыша), а также к какой-либо другой вакцине, которая содержит дифтерийный анатоксин.
Особые указания и меры предосторожности
Перед вакцинацией Превенар 20 проконсультируйтесь с лечащим врачом, если у Вас или Вашего ребёнка:
- присутствуют в настоящее время или возникали в прошлом какие-либо медицинские проблемы после введения препарата Превенар 20, такие как аллергическая реакция или проблемы, связанные с дыханием;
- тяжёлое заболевание или высокая температура; однако лёгкая лихорадка или инфекция верхних дыхательных путей (например, простуда) сами по себе не являются основанием для отсрочки вакцинации;
- имеются проблемы со свёртыванием крови или легко образуются синяки;
- ослабленная иммунная система (например, по причине ВИЧ-инфекции), вы может не получить всей пользы от применения препарата Превенар 20;
- следует воздержаться от введения вакцины, если при первичной вакцинации выявлены тяжёлые формы аллергических реакций.
Как и любая вакцина Превенар 20 не обеспечивает защиту всех вакцинированных людей. Превенар® 20 будет обеспечивать защиту только против инфекций уха, вызванных серотипами Streptococcus pneumoniae, для которых была разработана вакцина. Препарат не будет обеспечивать защиту от других возбудителей инфекционных заболеваний, которые могут вызывать инфекции уха.
Дети и подростки
Если Ваш ребёнок родился глубоко недоношенным (на 28-й неделе беременности или ранее), сообщите об этом перед вакцинацией лечащему врачу, поскольку в течение 2-3 дней после вакцинации у ребёнка могут возникать более длинные, чем в норме паузы между дыхательными движениями. См. также раздел 4.
Другие препараты и препарат Превенар 20
Сообщите лечащему врачу о том, что Вы или Ваш ребёнок получает, недавно получал или может начать получать какие-либо другие препараты или недавно получили какую-либо другую вакцину.
Ваш ребёнок может получить Превенар 20 одновременно с другими стандартными детскими вакцинами, кроме вакцины от туберкулёза.
В соответствии с национальными рекомендациями допускается одновременное введение вакцины Превенар 20 с другими вакцинами Национального календаря профилактических прививок и прививок по эпидемическим показаниям (кроме БЦЖ) при условии их введения разными шприцами в разные участки тела. При необходимости допускается введение более одной вакцины в одну мышцу, при этом следует сделать отступ между местами инъекции в 2,5–3 см, чтобы в случае возникновения местной реакции была возможность дифференцировать, какая вакцина её вызвала. При необходимости раздельного (не в один календарный день) введения вакцины Превенар 20 и других вакцин, допустим любой интервал между введениями, т.к. вакцина Превенар 20 является инактивированной.
У взрослых Превенар 20 можно вводить одновременно с вакциной против гриппа (инактивированная вакцина против гриппа) в разные места инъекций. В зависимости от оценки индивидуального риска вашим врачом может быть рекомендовано провести иммунизацию в разные дни, например, с интервалом в 4 недели.
Беременность, грудное вскармливание и фертильность
Если Вы беременны или кормите грудью, думаете, что забеременели или планируете беременность, перед началом применения препарата проконсультируйтесь с лечащим врачом.
Управление транспортными средствами и работа с механизмами
Превенар 20 не оказывает или оказывает незначительное влияние на способность управлять автотранспортными средствами и работать с механизмами. Однако, некоторые из реакций, упомянутых в разделе 4, могут оказывать влияние на способность управлять автотранспортным средством и работать с механизмами.
Препарат Превенар 20 содержит
Препарат Превенар 20 содержит натрий в концентрации менее 1 ммоль натрия (23 мг) на дозу, то есть практически не содержит натрия.
3. Применение препарата Превенар 20
Рекомендуемая доза
Применение у взрослых
Взрослые должны получить одну инъекцию.
Особые группы пациентов
Лица, считающиеся подверженными более высокому риску пневмококковой инфекции (например, лица с серповидноклеточной анемией или ВИЧ-инфекцией), включая лиц, ранее получавших вакцинацию 23-валентной пневмококковой полисахаридной вакциной, могут получить как минимум одну дозу препарата Превенар 20.
Лица, которым была выполнена трансплантация кроветворных стволовых клеток, могут получить три инъекции: первую через 3-6 месяцев после трансплантации и с интервалом не менее 4 недель между дозами. Выполнение четвертой инъекции — ревакцинации рекомендуется осуществлять через 6 месяцев после получения третьей инъекции. Сообщите лечащему врачу, если Вы ранее получали инъекцию пневмококковой вакцины. Если у Вас возникли дополнительные вопросы по применению препарата Превенар 20, проконсультируйтесь с лечащим врачом.
Применение у детей и подростков
Младенцы в возрасте от 6 недель до 15 месяцев
Ваш ребёнок может получить курс из трех инъекций в соответствии с официальными рекомендациями, или медицинский работник может использовать альтернативную схему (курс из четырёх инъекций: три инъекции на первом году жизни и ревакцинации в возрасте от И до 15 месяцев). Важно придерживаться инструкций лечащего врача или медсестры, чтобы завершить полный курс инъекций.
- Первая инъекция может быть выполнена в возрасте 6 недель.
- Каждая инъекция будет проводиться с интервалом приблизительно в два месяца, за исключением последней инъекции — ревакцинации, которая будет вводиться в возрасте от 11 до 15 месяцев.
- Вам сообщат, когда Вашему ребёнку следует прийти для получения следующей инъекции.
Недоношенные младенцы (рождённые до 37-й недели беременности)
- Ваш ребёнок получит начальный курс из трех инъекций. Первая инъекция может проводиться уже в возрасте 6 недель с промежутком как минимум один месяц между дозами. В возрасте от 11 до 15 месяцев Ваш ребёнок получит четвертую инъекцию — ревакцинацию.
Вам сообщат, когда Вашему ребёнку следует прийти для получения следующей инъекции.
Невакцинированные младенцы и дети старше 7 месяцев
- Младенцы в возрасте от 7 до 12 месяцев должны получить три инъекции. Первые две вводятся с интервалом по меньшей мере 4 недели. Третья инъекция — ревакцинация будет выполнена на втором году жизни, но не ранее чем через 2 месяца после введения второй дозы.
- Дети в возрасте от 12 до 24 месяцев должны получить две инъекции с интервалом по меньшей мере 8 недель.
- Дети в возрасте от 2 до 5 лет должны получить одну инъекцию.
Младенцы, дети и подростки, ранее вакцинированные пневмококковой конъюгированной вакциной
Младенцы и дети, которые ранее получали пневмококковую конъюгированную вакцину, могут получить Превенар 20 для завершения полного курса инъекций на любом из этапов схемы.
- Дети в возрасте от 15 месяцев до 5 лет, должны получить одну дозу (0,5 мл) препарата Превенар 20.
- Дети и подростки в возрасте от 5 до 18 лет рекомендована одна инъекция Превенар 20.
Важно придерживаться инструкций лечащего врача таким образом, чтобы Ваш ребёнок получил полный рекомендуемый курс вакцинации. В противном случае Ваш ребёнок может быть не полностью защищён от заболевания.
Если Ваш ребёнок пропускает инъекцию, важно, чтобы Вы записались на другое время. Это необходимо для того, чтобы Вы и Ваш врач могли обсудить меры, которые необходимо предпринять для защиты Вашего ребёнка.
Путь и (или) способ введения
Врач или медицинская сестра сделает инъекцию рекомендуемой дозы (0,5 мл) вакцины в мышцу Вашего плеча или в мышцу плеча или бедра Вашего ребёнка. При невозможности введения в дельтовидную мышцу — препарат вводят в латеральную широкую мышцу бедра (в средней трети).
4. Возможные нежелательные реакции
Подобно всем лекарственным препаратам препарат Превенар 20 может вызывать нежелательные реакции, однако они возникают не у всех.
Серьёзные нежелательные реакции препарата Превенар 20
Немедленно сообщите врачу, если Вы заметили у себя признаки следующих серьёзных побочных реакций (см. также раздел 2):
припухлость лица, губ, рта, языка или горла (отёк), затруднение дыхания, хрипы — это может быть признаком тяжёлой аллергической реакции, такой как анафилаксия, включая шок.
Другие нежелательные реакции
Следующие нежелательные реакции были зарегистрированы для препарата Превенар 20 у младенцев и детей (в возрасте от 6 недель до 5 лет)
Очень часто: могут возникать у более чем 1 человека из 10
- Снижение аппетита
- Раздражительность
- Сонливость
- Повышение температуры тела
- В месте инъекции для всех детей: покраснение, припухлость или уплотнение, боль или болезненность
- В месте инъекции после ревакцинации и у детей в возрасте от 2 до 5 лет: покраснение,
припухлость или уплотнение размером более 2,0-7,0 см.
Часто: могут возникать не более чем у 1 человека из 10
- Жидкий стул
- Рвота
- Сыпь
- Высокая температура тела 38,9 °C или выше
- В месте инъекции после начального курса инъекций: покраснение, уплотнение, припухлость размером более 2,0-7,0 см.
Нечасто: могут возникать не более чем у 1 человека из 100
- Непроизвольное приступообразное сокращение мышц (судороги), в том числе вызванные высокой температурой тела
- Аллергическая сыпь (крапивница или сыпь, напоминающая крапивницу)
- В месте инъекции: покраснение, припухлость или уплотнение размером более 7,0 см; боль или болезненность, затрудняющие движения.
Редко: могут возникать не более чем у 1 человека из 1000
- Аллергическая реакция (гиперчувствительность) в месте инъекции.
Неизвестно: исходя из имеющихся данных частоту возникновения определить невозможно
- Коллапс или шокоподобное состояние (гипотонический-гипореактивный эпизод)
- Аллергическая реакция (реакция гиперчувствительности), включая припухлость лица и/или губ
- Плач
- Беспокойный сон.
Следующие нежелательные реакции были зарегистрированы для препарата Превенар 20 у детей и подростков (в возрасте от 5 до 18 лет)
Очень часто: могут возникать у более чем 1 человека из 10
- Головная боль
- Боль в мышцах
- В месте инъекции: боль, болезненность, покраснение, припухлость или уплотнение
- Усталость, слабость
Часто: могут возникать не более чем у 1 человека из 10
- Боль в суставах
- В месте инъекции: боль или болезненность, затрудняющие движение.
Нечасто: могут возникать не более чем у 1 человека из 100
- Аллергическая сыпь (крапивница или сыпь, напоминающая крапивницу)
- Повышение температуры тела.
Неизвестно: исходя из имеющихся данных частоту возникновения определить невозможно
- Жидкий стул
- Рвота
- Снижение аппетита
- Раздражительность
- Сонливость
- Беспокойный сон
- Сыпь.
У детей и подростков с ВИЧ-инфекцией, серповидноклеточной анемией или трансплантацией кроветворных стволовых клеток наблюдались аналогичные побочные реакции, однако головные боли, рвота, жидкий стул, повышение температуры тела, повышенная утомляемость и слабость, боли в суставах и мышцах регистрировались очень часто.
У глубоко недоношенных младенцев (рождённых на 28 неделе беременности или ранее) более длинные промежутки между дыхательными движениями, чем в норме, могут возникать в течение 2–3 дней после вакцинации.
В ходе пострегистрационного применения препарата Превенар 13 у детей наблюдались следующие нежелательные реакции, которые также могут наблюдаться при применении препарата Превенар 20
- Тяжёлые аллергические реакции, включая шок (сердечно-сосудистый коллапс); отёк губ, лица или горла (ангионевротический отёк)
- Увеличение лимфатических узлов или желёз (лимфаденопатия) около места инъекции, например в подмышках или в паху
- В месте инъекции: аллергическая сыпь (крапивница), покраснение и раздражение (дерматит), а также зуд
- Сыпь в виде зудящих пятен красного цвета (многоформная эритема).
Следующие нежелательные реакции были зарегистрированы при применении препарата Превенар 20 у взрослых
Очень часто: могут возникать у более чем 1 человека из 10
- Головная боль
- Боль в суставах и в мышцах
- Боль/болезненность в месте инъекции и повышенная утомляемость.
Часто: могут возникать не более чем у 1 человека из 10
- Отёк в месте инъекции, покраснение в месте инъекции и повышение температуры тела.
Нечасто: могут возникать не более чем у 1 человека из 100
- Жидкий стул, тошнота и рвота.
- Сыпь и отёк лица, губ, рта, языка или горла, которые могут вызвать затруднения при глотании или дыхании (ангионевротический отёк).
- Зуд в месте инъекции, увеличение лимфоузлов в области шеи, подмышек или паха (лимфаденопатия), крапивница в месте инъекции, озноб.
Следующие нежелательные реакции наблюдались при использовании препарата Превенар 13 и могут также наблюдаться при использовании препарата Превенар 20
- Сыпь в виде зудящих пятен красного цвета (многоформная эритема)
- Раздражение в месте инъекции
- Снижение аппетита
- Ограничение движений руки.
Сообщение о нежелательных реакциях
Если у Вас возникают какие-либо нежелательные реакции, проконсультируйтесь с врачом, работником аптеки или медицинской сестрой. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в листке- вкладыше. Вы также можете сообщить о нежелательных реакциях напрямую через систему сообщений государств — членов Евразийского экономического союза (см. ниже). Сообщая о нежелательных реакциях, Вы помогаете получить больше сведений о безопасности препарата.
Российская Федерация
Федеральная служба по надзору в сфере здравоохранения
Адрес: 109012, Москва, Славянская площадь, д.4, стр.1.
Тел.: +7 800 550 99 03
Электронная почта: pharm@roszdravnadzor.gov.ru
Сайт в информационно-телекоммуникационной сети «Интернет»: http://www.roszdravnadzor.gov.ru
Республика Армения
«Центр экспертизы лекарств и медицинских технологий» ГНКО
Адрес: 0051, г. Ереван, пр. Комитаса 49/5
Телефон: +374 (10) 23-16-82, 23-08-96; +374 (60) 83 00 73
Электронная почта: info@ampra.am
Сайт в информационно-телекоммуникационной сети «Интернет»: http://www.pharm.am
Республика Казахстан
РГП на ПХВ «Национальный центр экспертизы лекарственных средств и медицинских изделий» Комитета медицинского и фармацевтического контроля Министерства здравоохранения Республики Казахстан
Адрес: 010000, г. Астана, район Байконыр, ул. А. Иманова 13, (БЦ «Нурсаулет 2»)
Тел.: +7 (7172)235-135
Электронная почта: farm@dari.kz
Сайт в информационно-телекоммуникационной сети «Интернет»:http://www.ndda.kz
Кыргызская Республика
Департамент лекарственных средств и медицинских изделий при Министерстве здравоохранения Кыргызской Республики
Адрес: 720044, г. Бишкек, ул. 3-я Линия, 25
Тел.:+996 (312)21-05-08
Электронная почта: vigilance@dlsmi.kg
Сайт в информационно-телекоммуникационной сети «Интернет»: http://www.dlsmi.kg
Республика Беларусь
УП «Центр экспертиз и испытаний в здравоохранении» Министерства здравоохранения Республики Беларусь
Адрес: 220037, г. Минск, Товарищеский пер. 2а
Телефон отдела фармаконадзора: +375 (17) 242-00-29
Электронная почта: rcpl@rceth.by
Сайт в информационно-телекоммуникационной сети «Интернет»:http://www.rceth.by
5. Хранение препарата Превенар 20
Храните препарат в недоступном для ребёнка месте так, чтобы ребёнок не мог увидеть его.
Не применяйте препарат после истечения срока годности (срока хранения), указанного на упаковке или на этикетке шприца после «Годен до».
Датой истечения срока годности является последний день данного месяца.
Хранить в холодильнике (2–8 °C). Не замораживать.
Предварительно наполненные шприцы следует хранить в холодильнике в горизонтальном положении, чтобы свести к минимуму время ресуспендирования.
Если препарат был заморожен, его следует утилизировать.
Препарат Превенар 20 следует использовать как можно скорее после извлечения из холодильника.
Данные по стабильности показывают, что препарат стабилен в течение 96 часов при хранении при температуре от 8 до 25 °C или в течение 72 часов при хранении при температуре от 0 до 2 °C. К концу этих сроков препарат Превенар 20 должен быть уже использован или его следует утилизировать.
Эти данные являются рекомендациями для медицинских работников только на случай временных температурных отклонений.
Уточните у врача, медицинской сестры или фармацевта, как следует утилизировать препарат, который больше не потребуется. Эти меры позволят защитить окружающую среду.
6. Содержимое упаковки и прочие сведения
Препарат Превенар 20 содержит:
1 доза (0,5 мл) содержит:
- по 2,2 мкг каждого из Streptococcus pneumoniae серотипа 1,3,4, 5, 6A,7F, 8, 9V, 10А, 11 A 12F 14, 15В, 18C, 19A, 19F, 22F, 23F и 33F, полисахарид1
- 4,4 мкг Streptococcus pneumoniae серотипа 6B, полисахарид1
1 конъюгированные с белком-носителем CRM197 (приблизительно 51 мкг на дозу) и адсорбированные на алюминия фосфате (0,125 мг алюминия на дозу).
Вспомогательные вещества:
Сведения об адъюванте указаны в разделе 2.
Внешний вид препарата Превенар 20 и содержимое упаковки
Препарат представляет собой гомогенную суспензию белого цвета для внутримышечного введения 0,5 мл.
По 0,5 мл в шприц вместимостью 1 мл из бесцветного стекла (тип I).
Шприц с препаратом в комплекте с иглой помещают в герметичный термоформованный лоток. 1 лоток вместе с листком-вкладышем помещают в картонную пачку с контролем первого вскрытия или
5 шприцев помещают в герметичный термоформованный лоток. 2 лотка по 5 шприцев и 10 игл в контурной упаковке вместе с листком-вкладышем помещают в картонную пачку с контролем первого вскрытия.
Держатель регистрационного удостоверения
Соединённые Штаты Америки
Пфайзер Инк.
66 Hudson Boulevard East,
New York, NY 10001-2192, USA
Тел: +1 (212) 733-23-23
https://www.pfizer.com/contact/email
Производитель
Пфайзер Айрлэнд Фармасьютикалз, Ирландия
Grange Castle Business Park, Clondalkin, Dublin 22, Ireland
Упаковщик/выпускающий контроль качества
Пфайзер Мэнюфэкчуринг Бельгия НВ, Бельгия
Rijksweg 12, Puurs-Sint-Amands, 2870, Belgium
Перечень представителей держателя регистрационного удостоверения на территории Союза
За любой информацией о препарате, а также в случаях возникновения претензий следует обращаться к местному представителю держателя регистрационного удостоверения:
Республика Беларусь
Представительство Частной компании с ограниченной ответственностью «Pfizer Export B.V.» (Королевство Нидерландов) в Республике Беларусь
Адрес: 22003 6, Минск, пр. Дзержинского 8, офис 403
Тел.: +375 (17) 309-38-00
Факс: +375 (17) 309-38-19
Электронная почта: belarusro@pfizer.com
Российская Федерация (а также для Республики Армения и Кыргызской Республики)
ООО «Пфайзер Инновации»
Адрес: 123112, Москва, Пресненская наб., д. 10, БЦ «Башня на Набережной» (Блок С)
Тел.: +7 (495) 287-50-00
Факс: +7 (495) 287-53-00
Электронная почта: Russia@pfizer.com
Республика Казахстан
Филиал компании Pfizer Export B.V. (Пфайзер Экспорт Би.Ви.) в Республике Казахстан
Адрес: 050000, г. Алматы, Медеуский район, проспект Нурсултана Назарбаева, д. 100/4
Тел.: +7(727)250 09 16
Факс: +7 (727) 250 42 09
Электронная почта: PfizerKazakhstan@pfizer.com
Листок-вкладыш пересмотрен:
Прочие источники информации
Подробные сведения о данном препарате содержатся на веб-сайте Союза http://eec.eaeunion.org/.
Представленные данные о лекарственном препарате будут дополняться новыми сведениями и по мере необходимости листок-вкладыш будет обновляться.
(линия отрыва или отреза)
Следующие сведения предназначены исключительно для медицинских работников:
Во время хранения может наблюдаться образование белого осадка и прозрачной надосадочной жидкости. Это не является признаком ухудшения качества препарата.
Предварительно наполненные шприцы следует хранить в горизонтальном положение чтобы свести к минимуму время ресуспендирования.
Подготовка к введению препарата
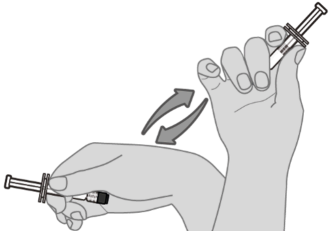
Этап 1. Ресуспендирование вакцины
Удерживайте предварительно наполненный шприц горизонтально между большим и указательным пальцами и энергично встряхивайте, пока содержимое шприца не превратится в гомогенную суспензию белого цвета. Не используйте вакцину, если её не удаётся ресуспендировать.
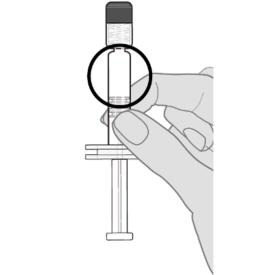
Этап 2. Визуальная оценка
Перед введением препарата визуально осмотрите его на наличие крупных механических включений или изменения цвета. Не используйте препарат, если обнаружены крупные механические включения или изменение цвета. Если вакцина не представляет собой гомогенную суспензию белого цвета, повторите этапы 1 и 2.
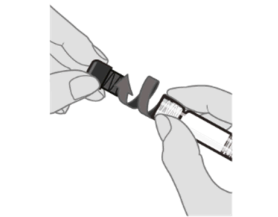
Этап 3. Снимите колпачок шприца
Снимите колпачок шприца с адаптера с люэровским соединением, медленно поворачивая колпачок против часовой стрелки, удерживая адаптер с люэровским соединением.
Примечание. Следует соблюдать осторожность, чтобы исключить нажатие на выдвинутый шток поршня при снятии колпачка со шприца.
Этап 4. Присоедините стерильную иглу
Присоедините иглу, предназначенную для внутримышечного введения, к предварительно наполненному шприцу, удерживая адаптер с люэровским соединением и поворачивая иглу по часовой стрелке.
Вводите всю дозу целиком.
Превенар 20 предназначен только для внутримышечного введения.
Превенар 20 запрещается смешивать с какими-либо другими вакцинами в одном шприце.
Превенар 20 можно применять одновременного с другими детскими вакцинами. При одновременном применении вакцины следует вводить в разные места.
Превенар 20 можно применять у взрослых одновременно с вакциной против сезонного гриппа (4-валентной вакциной, на основе поверхностных антигенов, инактивированной, адъювантной). У лиц с сопутствующими заболеваниями, связанными с высоким риском развития угрожающей жизни пневмококковой инфекции, может быть рассмотрен вопрос
об отдельном введении 4-валентной гриппозной вакпины и вакцины Превенар20 (например, с интервалом около 4 недель). Вакцины следует вводить в разные места.
Неиспользованный остатки препарата или отходы материалов следует утилизировать в соответствии с локальными требованиями.
Форма выпуска
Суспензия для внутримышечного введения, 0,5 мл.
Условия отпуска из аптек
Отпускают по рецепту
Классификация
-
Фармакотерапевтическая группа
-
АТХ
-
Действующее вещество
Подробнее по теме
Ознакомьтесь с дополнительными сведениями о препарате Превенар 20:
