Нинларо®
Ninlaro®Регистрационный номер
Торговое наименование
Международное непатентованное наименование
Лекарственная форма
капсулы
Фармакотерапевтическая группа
Код АТХ
Листок-вкладыш — информация для пациента
НИНЛАРО®, 2,3 мг, капсулы
НИНЛАРО®, 3 мг, капсулы
НИНЛАРО®, 4 мг, капсулы
Действующее вещество: иксазомиб
▼ Лекарственный препарат подлежит дополнительному мониторингу, который способствует быстрому выявлению новых сведений о безопасности. Это позволит в короткий срок выявить новую информацию о безопасности. Обращаемся к работникам системы здравоохранения с просьбой сообщать о любых подозреваемых нежелательных реакциях.
Способ сообщения о нежелательных реакциях представлен в разделе 4 настоящего листка-вкладыша.
Перед приёмом препарата полностью прочитайте листок-вкладыш, поскольку в нем содержатся важные для Вас сведения.
- Сохраните листок-вкладыш. Возможно, Вам потребуется прочитать его ещё раз.
- Если у Вас возникли дополнительные вопросы, обратитесь к лечащему врачу или медицинской сестре.
- Препарат назначен именно Вам. Не передавайте его другим людям. Он может навредить им, даже если симптомы их заболевания совпадают с Вашими.
- Если у Вас возникли какие-либо нежелательные реакции, обратитесь к лечащему врачу или медицинской сестре. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в разделе 4 листка-вкладыша.
Содержание листка-вкладыша
- Что из себя представляет препарат Нинларо® и для чего его применяют.
- О чём следует знать перед приемом препарата Нинларо®.
- Приём препарата Нинларо®.
- Возможные нежелательные реакции.
- Хранение препарата Нинларо®.
- Содержимое упаковки и прочие сведения.
1. Что из себя представляет препарат Нинларо® и для чего его применяют
Препарат Нинларо® содержит действующее вещество иксазомиб, который относится к группе препаратов под названием: «противоопухолевое средство».
Препарат Нинларо® используется для лечения опухоли костного мозга — множественной миеломы. Действующее вещество, содержащееся в препарате, блокирует действие протеасом. Протеасомы представляют собой структуры внутри клетки, разрушающие белки и являющиеся важными для жизнеспособности клеток. Поскольку миеломные клетки вырабатывают много белков, блокирование действия протеасом может разрушать опухолевые клетки.
Показания к применению
Препарат Нинларо® показан у взрослых в комбинации с леналидомидом и дексаметазоном для лечения пациентов с множественной миеломой, получавших ранее как минимум одну линию предшествующей терапии.
Что такое множественная миелома
Множественная миелома — это злокачественное заболевание крови, поражающее клетки, которые называются плазматическими. Плазматическая клетка — это клетка крови, которая в нормальном состоянии вырабатывает белки (иммуноглобулины) для борьбы с инфекциями. При множественной миеломе нормальные плазматические клетки превращаются в злокачественные клетки миеломы, которые способствуют разрушению костной ткани. Патологический (ненормальный) белок, вырабатываемый миеломными клетками в большом количестве может повредить почки. Лечение множественной миеломы подразумевает уничтожение миеломных клеток и уменьшение симптомов заболевания.
Если улучшение не наступило или Вы чувствуете ухудшение, необходимо обратиться к врачу.
2. О чём следует знать перед приёмом препарата Нинларо®
Противопоказания
Не принимайте препарат Нинларо®:
Если у Вас аллергия на иксазомиб или любые другие компоненты препарата (перечисленные в разделе 6 листка-вкладыша);
Если Вы не уверены, относятся ли вышеописанные условия к Вам, обратитесь к Вашему лечащему врачу прежде, чем начать приём Нинларо®.
Особые указания и меры предосторожности
Перед приёмом препарата Нинларо® проконсультируйтесь с лечащим врачом. Сообщите Вашему лечащему врачу прежде, чем начать приём Нинларо®, если:
- у Вас имеются или были в прошлом кровотечения; если у Вас снижено количество тромбоцитов (по анализу крови);
- у Вас постоянная тошнота, рвота или диарея;
- у Вас имеются или были в прошлом неврологические проблемы, включая онемение, ощущение покалывания и жжения кожи рук или ног;
- у Вас имеется или был в прошлом отёк (периферический отёк);
- у Вас наблюдается постоянная сыпь;
- у Вас имеются или были в прошлом проблемы с печенью или почками, поскольку Вам может потребоваться изменение дозы;
- у Вас имеются судороги, гипертензия, головная боль, нарушение сознания и нарушение зрения, Вам могут потребоваться дополнительные исследования и, возможно, отмена терапии
Ваш врач осмотрит Вас, также Вы будете находиться под наблюдением во время лечения. До начала приёме препарата Нинларо® и в ходе лечения Вы будете сдавать анализы крови, в том числе для проверки наличия достаточного количества клеток крови.
Дети и подростки
Не давайте препарат детям от 0 до 18 лет вследствие риска неэффективности и вероятной небезопасности (безопасность и эффективность применения иксазомиба у детей в возрасте до 18 лет не установлены).
Другие препараты и препарат Нинларо®
Сообщите лечащему врачу о том, что Вы принимаете, недавно принимали или можете начать принимать какие-либо другие препараты. Сюда относятся любые безрецептурные лекарственные препараты, такие как витамины или лекарственные препараты растительного происхождения. Сообщать о приёме данных препаратов необходимо, поскольку они могут повлиять на действие препарата Нинларо®. Сообщите Вашему лечащему врачу если Вы принимаете какие-либо из следующих препаратов: карбамазепин, фенитоин, рифампицин или зверобой продырявленный (Hypericum perforatum). Следует избегать приёме данных препаратов, поскольку они могут снизить эффективность Нинларо®.
Беременность и грудное вскармливание
Если Вы беременны или думаете, что забеременели, или планируете беременность, или кормите грудью, перед началом применения препарата проконсультируйтесь с лечащим врачом.
Применение лекарственного препарата Нинларо® во время беременности не рекомендовано, поскольку он может нанести вред Вашему будущему ребёнку. Во время приема Нинларо® кормление грудью следует прекратить.
Избегайте наступление беременности и кормление грудью во время приёме препарата Нинларо®.
Если Вы женщина детородного возраста или мужчина, который может стать отцом ребёнка, Вы должны использовать надёжные методы контрацепции во время лечения препаратом и в течение 90 дней после завершения лечения. Женщины, использующие гормональные контрацептивы, должны дополнительно использовать барьерный метод контрацепции. Немедленно сообщите врачу о наступлении беременности во время приёма препарата Нинларо® у Вас или Вашего полового партнёра.
Поскольку препарат Нинларо® назначают в комбинации с леналидомидом, следует придерживаться программы по предупреждению беременности для леналидомида, поскольку леналидомид может нанести вред Вашему будущему ребёнку.
Смотрите листки-вкладыши для леналидомида и дексаметазона для получения дополнительной информации о приёме во время беременности и кормления грудью.
Управление транспортными средствами и работа с механизмами
Приём препарата Нинларо® может повлиять на способность к управлению транспортными средствами и работе с механизмами. Вы можете почувствовать усталость и головокружение при приёме Нинларо®. Если у Вас возникли данные нежелательные реакции, не следует управлять транспортными средствами и работать с механизмами.
3. Приём препарата Нинларо®
Препарат Нинларо® назначается врачом, имеющим опыт лечения множественной миеломы. Всегда принимайте препарат в полном соответствии с рекомендациями Вашего лечащего врача.
Рекомендуемая доза: 1 капсула (4 мг) внутрь 1 раз в неделю (в один и тот же день недели) в течение первых 3 недель курса.
Нинларо® применяют в комбинации с леналидомидом (препарат, влияющий на работу иммунной системы) и дексаметазоном (противовоспалительный препарат).
Рекомендованная доза леналидомида составляет 25 мг каждый день в течение первых 3 недель курса.
Рекомендуемая доза дексаметазона составляет 40 мг 1 раз в неделю (в один и тот же день недели) в течение всех 4 недель курса.
Нинларо®, леналидомид и дексаметазон принимают в течение курсов лечения длительностью по 4 недели.
Схема приёма: Нинларо® в комбинации с леналидомидом и дексаметазоном
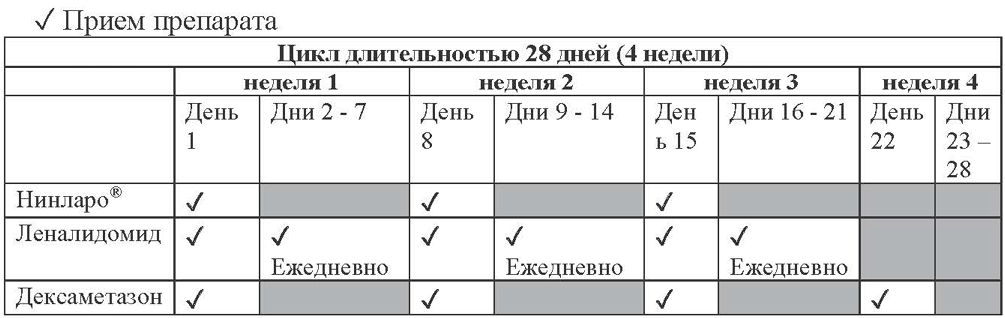
Вам следует прочитать листки-вкладыши для этих препаратов для получения более подробной информации об их применении и действии.
Если у Вас есть нарушения со стороны печени и почек, Ваш врач может прописать Вам приём капсул Нинларо® с дозировкой 3 мг.
Если у Вас возникли нежелательные реакции, Ваш врач может прописать вам приём капсул Нинларо® с дозировкой 3 мг или 2,3 мг.
Также врач может изменить дозы других принимаемых Вами препаратов.
Как и когда принимать препарат Нинларо®
- Принимайте Нинларо® минимум за 1 час или не ранее, чем через 2 часа после приема пищи.
- Проглатывайте капсулу целиком, запивая водой. Капсулу не раздавливать, не жевать и не открывать.
- Не допускать попадания содержимого капсулы на кожу. Если порошок случайно попал на кожу, следует тщательно смыть его с мылом и водой. Если капсула сломалась, осторожно убрать порошок, чтобы он не образовывал пыли в воздухе.
Если Вы приняли препарат Нинларо® больше, чем следовало
Если Вы превысили дозировку препарата Нинларо®, сообщите об этом врачу или сразу же обратитесь в больницу. Возьмите с собой упаковку препарата.
Если Вы забыли принять препарат Нинларо®
В случае задержки или пропуска приёма очередной дозы препарат следует принять, только если до приёма следующей запланированной дозы осталось более 3 дней или 72 ч. Пропущенную дозу не принимать менее чем за 72 ч перед приёмом следующей запланированной дозы.
В случае возникновения у Вас рвоты после приёма препарата, не следует принимать дополнительную дозу. Принимайте препарат как запланировано со следующей дозы.
Не принимайте двойную дозу, чтобы компенсировать пропущенную дозу.
Если Вы прекратили приём препарата Нинларо®
Следует продолжать лечение до тех пор, пока Ваш врач не скажет прекратить его.
При наличии вопросов по применению препарата обратитесь к лечащему врачу.
4. Возможные нежелательные реакции
Подобно всем лекарственным препаратам, препарат может вызывать нежелательные реакции, однако они возникают не у всех.
Если Вы заметите какие-либо из нижеуказанных очень частых серьёзных нежелательных реакций, которые могут возникнуть у более чем у 1
человека из 10 немедленно сообщите об этом Вашему врачу:
- низкое содержание тромбоцитов (тромбоцитопения) в анализе крови, это может повысить риск возникновения носовых кровотечений и образования синяков;
- тошнота, рвота и диарея;
- онемение, покалывание или жжение рук или стоп (периферическая нейропатия);
- отёк ног или ступней (периферический отёк);
- кожная сыпь, которая может сопровождаться зудом и возникать на нескольких участках по всему телу
Также, если Вы заметите какие-либо из нижеуказанных редких нежелательных реакций, которые могут возникать не более чем у 1 человека из 1000, немедленно сообщите об этом врачу:
- выраженная кожная сыпь в виде вздутий от красного до фиолетового цвета (синдром Свита) или кожная сыпь с шелушением кожи, образованием волдырей и язвами во рту (синдром Стивенса-Джонсона);
- мышечная слабость, потеря чувствительности пальцев ног или ступней, или потеря двигательных функций ног (поперечный миелит);
- изменения зрения, психического состояния или судороги (синдром задней обратимой энцефалопатии);
- быстрая гибель опухолевых клеток, которая может вызывать головокружение, уменьшение мочеиспускания, спутанность сознания, рвоту, тошноту, отеки, одышку, нарушения сердечного ритма (синдром лизиса опухоли);
- редкие состояния крови в результате образования тромбов, что может вызывать усталость, лихорадку, образование синяков, носовые кровотечения, уменьшение мочеиспускания (тромботическая тромбоцитопеническая пурпура)
Прочие возможные нежелательные реакции
Если какие-либо нижеуказанные нежелательные реакции станут серьёзными, сообщите об этом Вашему врачу.
Очень частые нежелательные реакции, которые могут возникать у более чем 1 человека из 10:
- запор;
- боль в спине;
- простудные симптомы (инфекция верхних дыхательных путей);
- чувство усталости или слабости (утомляемость);
- сниженное число белых кровяных телец — нейтрофилов (нейтропения), что может увеличивать риск инфекции;
- нежелание есть (пониженный аппетит);
- нарушение сердечного ритма (арить4ия>;
- нечёткость зрения, включая помутнение;
- сухость глаз;
- покраснение глаз (конъюнктивит).
Частые нежелательные реакции, которые могут возникать не более чем у 1 человека из 10:
- реактивация вируса ветряной оспы (опоясывающий герпес), вызывающий кожную сыпь и боль (опоясывающий лишай);
- пониженное артериальное давление (гипотензия);
- одышка, или непрекращающийся кашель, или хрипы (сердечная недостаточность);
- жёлтое прокрашивание глаз и кожи (желтуха, которая может являться симптомом печёночной недостаточности);
- низкое содержание калия в крови (гипокалиемия).
Сообщение о нежелательных реакциях
Если у Вас возникают какие-либо нежелательные реакции, в том числе не указанные в листке-вкладыше, проконсультируйтесь с врачом. К ним также относятся любые нежелательные реакции, не указанные в листке-вкладыше. Вы также можете сообщить о нежелательных реакциях напрямую (см. ниже). Сообщая о нежелательных реакциях, Вы помогаете получить больше сведений о безопасности препарата.
Республика Беларусь
Республиканское унитарное предприятие «Центр экспертиз и испытаний в здравоохранении»
220037, Минск, Товарищеский пер., 2а
Телефон: +375172995514
Факс: +375172995358
Электронная почта: rcpl@rceth.by
Адрес в интернете: www.rceth.by
Российская Федерация
Федеральная служба по надзору в сфере здравоохранения (РОСЗДРАВНАДЗОР)
109074, Москва, Славянская площадь, д. 4, строение 1
Телефон: 8 800 550 99 03
Факс: +74956981573
Электронная почта: pharm@roszdravnadzor.ru
Адрес в интернете: www.гоszdravnadzor.ru
Республика Армения
«Научный Центр экспертизы лекарств и медицинских технологий им.
Академика Э. Габриеляна» АОЗТ
0051, Ереван, пр. Комитаса 49/4
Телефон: +37410230896
Факс: +37410232118
Электронная почта: vigilance@pharm.am
Адрес в интернете: www.pharm.am
Республика Казахстан
РГП на ПХВ «Национальный Центр экспертизы лекарственных средств и медицинских изделий» Комитета контроля качества и безопасности товаров и услуг Министерства здравоохранения Республики Казахстан
010000, Нур-Султан, пр. Мацгилик Ел, 20
Тел.: +77172789899
Электронная почта: farm@dari.kz
Адрес в интернете: www.ndda.kz
Кыргызская Республика
Департамент лекарственного обеспечения и медицинской техники при Министерстве Здравоохранения Кыргызской Республики
720044, Бишкек, ул. 3-я Линия, 25
Горячая линия: 08008002626
Телефон: +996312219288
Факс: +996312210508
Электронная почта: dlomt@pharm.kg
Адрес в интернете: www.pharm.kg
5. Хранение препарата Нинларо®
Храните препарат в недоступном для ребёнка месте так, чтобы ребёнок не мог увидеть его.
Не применяйте препарат после истечения срока годности (срока хранения), указанного на блистере, картонной обложке, картонной пачке после слов «Годен до:».
Датой истечения срока годности является последний день данного месяца.
Храните при температуре не выше 25 °C. Не замораживайте. Храните в оригинальной упаковке непосредственно до приёма каждой капсулы.
Не извлекайте капсулу, если Вам не нужно принимать дозу.
Не применяйте препарат, если вы заметили какие-либо повреждения или признаки вскрытия упаковки.
Не выбрасывайте препараты в канализацию. Уточните у работника аптеки, как следует утилизировать (уничтожать) препарат, который больше не потребуется. Эти меры позволят защитить окружающую среду.
6. Содержимое упаковки и прочие сведения
Препарат Нинларо® содержит:
Нинларо®, 2,3 мг, капсулы:
- Действующим веществом является иксазомиб. Каждая капсула содержит 2,3 мг иксазомиба (в виде иксазомиба цитрата 3,29 мг).
- Прочими ингредиентами (вспомогательными веществами) являются: целлюлоза микрокристаллическая, тальк, магния стеарат;
оболочка капсулы: желатин, титана диоксид, краситель железа оксид красный, чернила черные 10А21.
Нинларо®, 3 мг, капсулы:
- Действующим веществом является иксазомиб. Каждая капсула содержит 3 мг иксазомиба (в виде иксазомиба цитрата 4,3 мг).
- Прочими ингредиентами (вспомогательными веществами) являются: целлюлоза микрокристаллическая, тальк, магния стеарат;
оболочка капсулы: желатин, титана диоксид, краситель железа оксид чёрный, чернила черные 10А21.
Нинларо®, 4 мг, капсулы:
- Действующим веществом является иксазомиб. Каждая капсула содержит 4 мг иксазомиба (в виде иксазомиба цитрата 5,7 мг).
- Прочими ингредиентами (вспомогательными веществами) являются: целлюлоза микрокристаллическая, тальк, магния стеарат;
оболочка капсулы: желатин, титана диоксид, краситель железа оксид красный, краситель железа оксид жёлтый, чернила черные 10А21.
1 Чернила черные 10А2 содержат: шеллак, пропиленглико ль, калия гидроксид, краситель оксид железа чёрный.
Внешний вид препарата Нинларо® и содержимое его упаковки
Нинларо® 2,3 мг, капсулы: твёрдые желатиновые капсулы № 4, корпус капсулы светло-розового цвета, крышечка капсулы светло-розового цвета, с надписями «Takeda» на крышечке капсулы и «2.3 mg» на корпусе капсулы, нанесёнными черными чернилами;
Нинларо® 3 мг, капсулы: твёрдые желатиновые капсулы № 4, корпус капсулы светло-серого цвета, крышечка капсулы светло-серого цвета, с надписями «Takeda» на крышечке капсулы и «3 mg» на корпусе капсулы, нанесёнными черными чернилами;
Нинларо® 4 мг, капсулы: твёрдые желатиновые капсулы № 3, корпус капсулы светло-оранжевого цвета, крышечка капсулы светло-оранжевого цвета, с надписями «Takeda» на крышечке капсулы и «4 mg» на корпусе капсулы, нанесёнными черными чернилами.
Содержимое капсул — порошок от белого до желтовато-белого цвета.
По 1 капсуле в блистере ПВХ Алюминий / Алюминий, вложенном в складывающуюся картонную обложку. По 1 картонной обложке вместе с листком-вкладышем помещают в пачку картонную. 3 картонные пачки помещают в общую картонную пачку. На защитной наклейке голо графическим способом указывают логотип «Takeda». и/или
По 1 капсуле в блистере ПВХ Алюминий / Алюминий, вложенном в складывающуюся картонную обложку. По 1 картонной обложке вместе с листком-вкладышем помещают в пачку картонную. На защитной наклейке голо графическим способом указывают логотип «Takeda».
Держатель регистрационного удостоверения
Таке да Фарма А/С, Дания
Takeda Pharma A/S, Denmark
Dybendal Alle 10,
DK-2630 Taastrup
Производитель
Хаупт Фарма Амарег ГмбХ, Германия
Haupt Pharma Arnareg GmbH, Germany
Donaustaufer Strasse 378,
93055 Regensburg
Выпускающий контроль качества
Таке да Айлэнд Лимитед, Ирландия
Takeda Ireland Limited, Ireland
Grange Castle Business Park,
Dublin 22, D22 XR57 или
ООО «Такеда Фармасьютикалс»
Россия, 150030, г. Ярославль,
ул. Техно парковая, д. 9
Тел.: (495) 933-55-11
Факс: (495) 502-16-25
в случае производства капсул 3 мг и 4 мг на ООО «Такеда Фармасьютикалс», Россия указывают:
Производитель
ООО «Такеда Фармасьютикалс»
Россия, 150030, г. Ярославль, ул. Техно парковая, д. 9 Тел.: (495) 933-55-11
Факс: (495) 502-16-25
За любой информацией о препарате, а также в случаях возникновения претензий следует обращаться к местному представителю держателя регистрационного удостоверения:
Республика Беларусь
Представительство ООО «Takeda Osteuropa Holding GmbH» (Австрийская Республика) в Республике Беларусь
220020, Минск, пр-т Победителей, 84, офис 27
Телефон: +375172404120
Факс: +375172404130
Электронная почта: DSO-BY@takeda.com
Российская Федерация
ООО «Такеда Фармасьютикалс»
119048, Москва, ул. Усачёва, д. 2, стр.1
Телефон: +74959335511
Факс: +74955021625
Электронная почта: rassia@takeda.com
Адрес в интернете: www.takeda.com/ra-ru
Республика Армения
«Такеда Австрия ГмбХ» Представительство в Республике Армения
0010, Ереван, ул. Терьяна, 105/1, бизнес-центр «Цитадель»
Телефон: +37410514880
Электронная почта: DSO-KZ@takeda.com
Республика Казахстан
ТОО «Такеда Казахстан»
050040, Алматы, ул. Шашкина 44
Телефон: +77272444004
Факс: + 77272444005
Электронная почта: DSO-KZ@takeda.com
Кыргызская Республика
Представительство Компании “Takeda Osteuropa Holding GmbH” (Австрия) в Кыргызской Республике
720014, Бишкек, Первомайский район, ул. Кудрука, 101
Телефон: +996312976895
Электронная почта: DSO-KZ@takeda.com
Листок-вкладыш пересмотрен
Форма выпуска
Капсулы 2,3 мг, 3 мг и 4 мг.
Условия отпуска из аптек
Отпускают по рецепту
Производитель
Haupt Pharma Amareg, GmbH, Германия
Такеда Фармасьютикалс, ООО, Российская Федерация
AndersonBrecon (UK) Limited, Великобритания
Подробнее по теме
Ознакомьтесь с дополнительными сведениями о препарате Нинларо:
