Варилрикс®
, вакцинаРегистрационный номер
Торговое наименование
Международное непатентованное наименование
Лекарственная форма
лиофилизат для приготовления раствора для подкожного введения
Состав
1 прививочная доза (0,5 мл) содержит4:
| Наименование компонентов | Количество |
| Действующее вещество | |
| Живой аттенуированный вирус Varicella Zoster (штамм Oka) | ≥ 103,3 БОЕ1,2 |
| Вспомогательные вещества | |
| Сывороточный альбумин человека3 Аминокислоты Неомицина сульфат Растворитель | 1 мг 32 мг 6 мг 8 мг 8 мг менее 25 мкг 0,5 мл |
Примечание:
1. БОЕ — бляшкообразующие единицы.
2. Номинальный титр вируса. Соответствует минимальному титру, гарантируемому производителем на дату окончания срока годности. С целью компенсации снижения титра вируса в течение срока годности препарата в состав введен избыток: на момент выпуска препарата 1 прививочная доза содержит ≥ 103,7 БОЕ.
3. Выполняет функцию стабилизатора.
4. Вакцина не содержит консервантов.
Описание
Фармакотерапевтическая группа
Фармакологические свойства
Фармакодинамика
Механизм действия
Введение вакцины Варилрикс® вызывает выработку антител к вирусу ветряной оспы, обеспечивая специфическую защиту от этой инфекции. Определённая степень защиты может быть достигнута при иммунизации в течение до 72 часов после контакта с вирусом Varicella Zoster. Титр антител ≥1/4, установленный методом непрямой реакции иммунофлюоресценции (НРИФ), считается протективным.
Иммунологическая эффективность
Здоровые лица
Практически у всех здоровых детей в возрасте от 9 месяцев до 12 лет включительно через шесть недель после вакцинации определялся уровень защиты, который сохранялся, по крайней мере, в течение 7 лет после вакцинации. Введение даже 1 дозы вакцины эффективно предотвращает 81 % всех госпитализаций у детей, связанных с заболеванием, и 87 % амбулаторных визитов. Тем не менее, у детей, получивших 1 дозу вакцины Варилрикс®, в сроки, превышающие 42 дня после прививки, регистрировались отдельные случаи заболевания, вызванного диким штаммом Varicella Zoster. Введение 2-ой дозы эффективно предотвращает случаи заражения ветряной оспой.
Все дети в возрасте от 13 лет после двукратной вакцинации имели выраженный уровень защиты, который сохранялся как минимум один год (во время наблюдения в рамках клинического исследования). В клинических исследованиях было показано, что большинство вакцинированных, находившихся впоследствии в контакте с заболевшими, либо не подвержены инфекции, либо переносят заболевание в значительно более лёгкой форме (меньшее количество высыпаний, отсутствие лихорадки).
Пациенты из групп высокого риска
Ветряная оспа представляет собой важный фактор риска, ухудшающий течение и прогноз имеющегося тяжёлого заболевания в следующих группах пациентов:
- пациенты с острым лейкозом;
- пациенты, получающие терапию иммунодепрессантами, включая применение кортикостероидов;
- пациенты, которым планируется произвести операцию трансплантации;
- пациенты, страдающие тяжёлыми хроническими заболеваниями, такими как метаболические и эндокринные расстройства, хронические заболевания лёгких и сердечно-сосудистой системы, муковисцидоз и нервно-мышечные нарушения;
- здоровые люди, находящиеся в тесном контакте с заболевшими или группами высокого риска, не болевшие ветряной оспой и не привитые ранее.
У пациентов из групп высокого риска следует периодически осуществлять определение титров антител к вирусу ветряной оспы для принятия решения о необходимости дополнительной прививки.
Показания
Противопоказания
Применение при беременности и в период грудного вскармливания
Способ применения и дозы
Способ введения
Препарат Варилрикс® предназначен для подкожного введения.
Варилрикс® нельзя вводить внутрисосудисто или внутрнкожно.
Предпочтительное место введения препарата Варилрикс® — дельтовидная область плеча. Растворитель и восстановленную вакцину перед использованием необходимо визуально проверить на отсутствие механических включений и/или изменение внешнего вида. В случае их обнаружения следует отказаться от применения растворителя или восстановленной вакцины. Восстановленный препарат представляет собой прозрачную жидкость от желто- розового до розового цвета, Восстановленный препарат не должен содержать осадок и видимые посторонние включения.
Варилрикс® нельзя смешивать в одном шприце с другими вакцинами.
Приготовление вакцины перед введением с использованием растворителя в шприце
Варилрикс® необходимо восстановить путём добавления полного объёма растворителя из предварительно наполненного шприца во флакон, содержащий лиофилизат.
Внимание! Упаковка препарата Варилрикс® может быть представлена двумя типами шприцев, различающихся по способу соединения иглы с носиком шприца.
Для правильного выбора способа соединения иглы и шприца, следуйте представленным ниже инструкциям.
Шприц 1 типа
Рисунок 1.
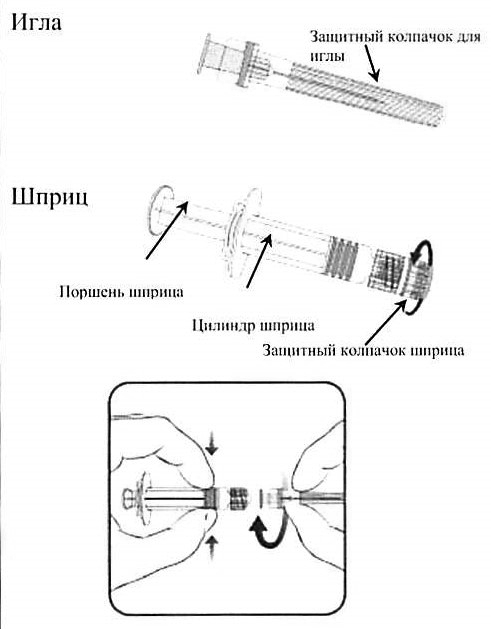
Инструкция по подготовке шприца 1 типа (рисунок 1) к использованию:
1. Открутите защитный колпачок шприца, поворачивая его против часовой стрелки (при этом следует удерживать шприц за цилиндр, избегая контакта с поршнем шприца).
2. Крутящим движением по часовой стрелке соедините иглу со шприцем до момента, когда вы ощутите их защелкивание друг на друге.
Удалите защитный колпачок с иглы (в отдельных случаях он может быть туго закреплен на игле).
Шприц 2 типа
В случае, если упаковка содержит шприц, отличный от представленного на рисунке 1, то после удаления защитного колпачка с носика шприца игла надевается на шприц до упора без дополнительного накручивания. Перенести растворитель из шприца во флакон с лиофилизатом. После добавления растворителя к лиофилизату хорошо встряхнуть образовавшуюся суспензию до полного растворения лиофилизата в растворителе (приблизительно 3 минуты). После восстановления вакцину необходимо незамедлительно ввести. Для введения вакцины следует использовать новую иглу. Для введения извлекают из флакона с восстановленной вакциной все его содержимое.
Приготовление вакцины перед введением с использованием растворителя в ампуле
Варилрикс® необходимо восстановить путём добавления полного объёма растворителя из ампулы во флакон, содержащий лиофилизат. После добавления растворителя к лиофилизату хорошо встряхнуть образовавшуюся суспензию до полного растворения лиофилизата в растворителе (приблизительно 3 минуты). После восстановления вакцину необходимо незамедлительно ввести. Для введения вакцины следует использовать новую иглу. Для введения извлекают из флакона с восстановленной вакциной все его содержимое.
После обработки места проведения инъекции спиртом или другим веществом, применяющимся для дезинфекции, следует подождать, пока это вещество испарится, поскольку мри контакте с подобными соединениями может произойти инактивация вакцинного вируса. Вакцину следует вводить сразу после её разведения растворителем. Неиспользованный препарат и отходы от его использования должны быть уничтожены в соответствии с требованиями, принятыми в РФ.
Схемы вакцинации
Плановая профилактика
По 1 дозе вакцины (0,5 мл) двукратно.
Рекомендованный минимальный интервал между прививками должен составлять 6 недель.
Экстренная профилактика
Вакцинацию проводят однократно 1 дозой вакцины (0,5 мл) в течение первых 96 часов после контакта (предпочтительно в течение первых 72 часов).
Вакцинация групп высокого риска
Пациенты с острым лейкозом, пациенты с тяжёлыми хроническими заболеваниями и пациенты, получающие терапию иммунодепрессантами и лучевую терапию
Иммунизация проводится в состоянии полной гематологической ремиссии. При этом необходимо удостовериться, что общее количество лимфоцитов составляет не менее 1200/мм3, а также отсутствуют симптомы, указывающие на недостаточность клеточного иммунитета.
Если вакцинацию планируется провести в острой фазе лейкоза, необходимо прервать химиотерапию на срок, равный одной неделе до и одной неделе после вакцинации. Не следует проводить вакцинацию в периоды лучевой терапии.
Пациенты, которым планируется произвести трансплантацию органа
Если пациентам предстоит трансплантация органа, то курс вакцинации должен быть завершен за несколько недель до начала проведения терапии иммунодепрессантами.
Пациентам групп высокого риска могут потребоваться дополнительные дозы вакцины. Решение о необходимости введения дополнительных доз препарата Варилрикс® принимает лечащим врач (иммуногематолог, онколог, трансплантолог).
Взаимозаменяемость вакцин
Варилрикс® может быть введен тем. кто уже был вакцинирован другой вакциной для профилактики ветряной оспы.
Курс вакцинации против ветряной оспы, начатый препаратом Варилрикс®, может быть продолжен другой вакциной для профилактики ветряной оспы.
Побочное действие
Нечасто: повышение температуры тела (ректальной ≥ 39,5 °C; в подмышечной впадине или ротовой полости: ≥ 39 °C), слабость, недомогание. Не было различий между профилем реактогенности у изначально серопозитивных и серонегативных лиц.
Пациенты из групп высокого риска
Существуют только ограниченные данные клинических исследований среди пациентов повышенного риска осложнённого течения ветряной оспы. Вакциноассоциированные реакции (в основном папуло-везикулезная сыпь и повышение температуры тела) имеют, как правило, лёгкое течение. Как н у здоровых лиц, покраснение, отёк и боль в месте инъекции имеют лёгкую степень и являются преходящими.
Данные пострегистрационного наблюдения
В ходе пострегистрационного наблюдения дополнительно зарегистрированы следующие нежелательные реакции после вакцинации.
Инфекционные и паразитарные заболевания
Редко: инфекция, вызванная Herpes Zoster.
Нарушения со стороны крови и лимфатической системы
Редко: тромбоцитопения.
Нарушения со стороны иммунной системы
Редко: реакции гиперчувствительности, анафилактические реакции.
Нарушения со стороны нервной системы
Редко: энцефалит, острое нарушение мозгового кровообращения, церебеллит, симптомы, напоминающие церебеллит (включая преходящее нарушение походки и преходящую атаксию), судороги.
Нарушения со стороны сосудов
Редко: васкулит (включая пурпуру Шонлейна-Геноха и синдром Кавасаки).
Нарушения со стороны кожи и подкожных тканей
Редко: многоформная эритема. При наблюдении за массовым применением вакцины зарегистрированы случаи анафилактоидных реакций.
Передозировка
Зарегистрированы отдельные сообщения о случайной передозировке вакцины. В некоторых из них сообщалось о развитии таких симптомов, как летаргия, судороги. В других случаях передозировка не привела к развитию нежелательных явлений.
Взаимодействие с другими лекарственными средствами
Здоровые лица
Варилрикс® может применяться одновременно с любыми другими вакцинами.
При применении с коревой вакциной, в случае если прививки не были сделаны в один день, рекомендуется интервал 30 дней.
Пациенты из групп высокого риска
Варилрикс® не следует назначать одновременно с другими живыми аттенуированными вакцинами, за исключением комбинированной вакцины против кори, краснухи и паротита. Однако если эти вакцины не были назначены одновременно, то интервал между их назначением для достижения максимального уровня антител должен составлять не менее 30 дней.
Особые указания
Влияние на способность управлять транспортными средствами, механизмами
Не установлено.
Форма выпуска
Лиофилизат для приготовления раствора для подкожного введения, 1 доза (0,5 мл).
Лиофилизат
По 1 дозе вакцины во флаконе из прозрачного стекла типа I (Евр. Ф.) вместимостью 3 мл, укупоренном пробкой из резины и алюминиевым колпачком под обкатку, снабжённым защитной пластиковой крышечкой.
Растворитель
По 0,5 мл в ампуле прозрачного стекла типа I (Евр. Ф.) вместимостью 1 мл. По 0,5 мл в шприце из прозрачного стекла типа I (Евр. Ф.) вместимостью 1,25 мл. Носик шприца герметично укупорен защитным резиновым колпачком или герметичной резиновой пробкой с защитным завинчивающимся пластиковым колпачком.
Комплектность
По 1 флакону с лиофилизатом, 1 ампуле с растворителем в блистере из поливинилхлорида, закрытом плёнкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 1 флакону с лиофилизатом, 1 шприцу с растворителем в блистере из поливинилхлорида, закрытом плёнкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 1 флакону с лиофилизатом, 1 шприцу с растворителем в комплекте с 1 иглой в отдельном пластиковом контейнере с канюлей, закрытой пластиковым колпачком, в блистере из поливинилхлорида, закрытом плёнкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 1 флакону с лиофилизатом, 1 шприцу с растворителем в комплекте с 2 иглами в отдельных пластиковых контейнерах с канюлями, закрытыми пластиковыми колпачками, в блистере из поливинилхлорида, закрытом плёнкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 100 флаконов с лиофилизатом с 1 или 10 инструкциями по применению в картонной коробке. По 25 ампул с растворителем в блистере из поливинилхлорида или полиэтилена, закрытом плёнкой или без плёнки. По 4 блистера в картонной коробке.
Хранение
Лиофилизат
Хранить при температуре от 2 до 8 °C. Хранить в защищённом от света месте.
Растворитель
Хранить при температуре от 2 до 25 °C. Не замораживать.
Комплект (лиофилизат, растворитель, с иглами или без игл)
Хранить при температуре от 2 до 8 °C. Не замораживать.
Хранить в защищённом от света месте. Хранить в недоступном для детей месте.
УСЛОВИЯ ТРАНСПОРТИРОВАНИЯ
Лиофилизат
Транспортировать при температуре от 2 до 8 °C.
Растворитель
Транспортировать при температуре от 2 до 25 °C. Не замораживать.
Комплект (лиофилизат, растворитель, с иглами или без игл)
Транспортировать при температуре от 2 до 8 °C. Не замораживать.
Срок годности
Условия отпуска из аптек
Отпускают по рецепту
Производитель
GlaxoSmithKline Biologicals, S.A., Бельгия
Подробнее по теме
Ознакомьтесь с дополнительными сведениями о препарате Варилрикс:
