Фазлодекс®
FaslodexРегистрационный номер
Торговое наименование
Международное непатентованное наименование
Лекарственная форма
раствор для внутримышечного введения
Состав
Один заполненный шприц содержит:
Активное вещество: 250 мг фулвестранта;
Вспомогательные вещества: этанол (96 %) 500 мг, бензиловый спирт 500 мг, бензилбензоат 750 мг, касторовое масло до 5 мл.
Описание
Прозрачная, от бесцветной до жёлтого цвета, вязкая жидкость.
Фармакотерапевтическая группа
Код АТХ
Фармакологические свойства
Фармакодинамика
Фулвестрант является конкурирующим антагонистом рецепторов эстрогена. По уровню аффинности к рецепторам сопоставим с эстрадиолом. Фулвестрант блокирует трофическое действие эстрогенов, не проявляя собственной эстрогеноподобной активности. Механизм действия связан с подавлением активности и деградацией эстроген-рецепторов (ЭР).
Также фулвестрант достоверно снижает экспрессию рецепторов прогестерона. Фулвестрант не оказывает стимулирующего эффекта на эндометрий у женщин в постменопаузе. Эффекты длительной терапии фулвестрантом на эндотелий, в постменопаузе не установлены. Также нет данных по морфологии эндометрия.
Данных о влиянии длительного применения фулвестранта на костную ткань нет.
Фармакокинетика
После внутримышечной инъекции фулвестрант медленно всасывается, достигая максимальной концентрации в плазме примерно через 7 дней. При использовании Фазлодекса в дозе 500 мг равновесное состояние достигается в течение первого месяца терапии (AUC 546 нг × день/мл, Cmax 25,1 нг/мл, Cmin 16,3 нг/мл). При равновесном состоянии содержание фулвестранта в плазме колеблется в относительно узких границах максимальные и минимальные показатели отличаются примерно в 3 раза.
После внутримышечной инъекции экспозиция примерно пропорциональна введённой дозе (в интервале доз от 50 до 500 мг).
Фулвестрант характеризуется экстенсивным и быстрым распределением. Большой, кажущийся объём распределения (от 3 до 5 л/кг) при равновесной концентрации предполагает преимущественно, экстраваскулярное распределение. Связь с белками плазмы — 99 %. Главные компоненты связывания включают фракции липопротеинов очень низкой плотности (ЛПОНП), липопротеинов низкой плотности (ЛПНП) и липопротеинов высокой плотности (ЛПВП). Роль связывающего половые гормоны глобулина не установлена.
Метаболизм фулвестранта включает комбинации множества потенциальных путей биотрансформации, аналогичных механизмам метаболизма эндогенных стероидов (включают метаболиты 17-кетон, сульфон, 3-сульфат, 3- и 17-глюкуронид). Идентифицированные метаболиты менее активны или равны по активности фулвестранту, CYP ЗA4 является единственным изоферментом из семейства P450, который участвует в окислении фулвестранта. Однако, представляется, что in vivo преобладают биотрансформации без участия P450.
Фулвестрант в основном выводится с фекалиями, с мочой выводится менее 1 % вещества. Клиренс фулвестранта составляет 11 ± 1,7 мл/мин/кг, что предполагает высокий уровень печёночной экстракции. Период полувыведения составляет 50 дней.
Особые популяции:
Фармакокинетический профиль фулвестранта не зависит от возраста (в диапазоне 33–89 лет), массы тела (40–127 кг) и расовой принадлежности.
Нарушения функции почек
Лёгкие и умеренные нарушения функции почек не оказывают клинически значимого влияния на фармакокинетику фулвестранта.
Нарушения функции печени
При однократном введении фулвестранта пациентам со слабым или умеренным нарушением функции печени (классы A и B по классификации Чайлд-Пью) отмечалось повышение AUC в 2,5 раза по сравнению со здоровыми добровольцами. Исследований фармакокинетики фулвестранта у пациентов с тяжёлыми нарушениями функции печени (класс C по классификации Чайлд-Пью) не проводилось.
Показания
Местно-распространённый или диссеминированный рак молочной железы с положительными рецепторами эстрогенов у женщин в постменопаузе при прогрессировании после или на фоне терапии антиэстрогенами.
Противопоказания
- Повышенная чувствительность к фулвестранту или любому другому компоненту препарата;
- тяжёлые нарушения функции печени;
- беременность и период кормления грудью;
- детский возраст до 18 лет.
С осторожностью
При нарушениях функции почек и печени.
Способ применения и дозы
Внутримышечно, путём медленной (в течение 1–2 мин) инъекции. Содержимое 2-х шприцев последовательно вводится в правую и левую ягодичные области.
Взрослые пациенты женского пола (включая пожилой возраст)
Рекомендуемая доза — 500 мг 1 раз в месяц. Первый месяц терапии: 500 мг 2 раза в месяц (второе введение — через 2 недели после первой дозы препарата).
Дети и подростки
Данных по безопасности и эффективности у детей и подростков нет.
Пациенты с нарушениями функции почек
В случаях лёгкого или умеренного нарушения функции почек (клиренс креатинина >30 мл/мин) коррекции дозы не требуется. Безопасность и эффективность препарата у пациентов с тяжёлыми нарушениями функции почек (клиренс креатинина <30 мл/мин) не установлены.
Пациенты с нарушениями функции печени
Применение препарата Фазлодекс® у пациентов с лёгким или умеренным нарушением функции печени не требует коррекции дозы. Однако, применение препарата Фазлодекс® у этой группы пациентов требует осторожности. Безопасность и эффективность препарата у пациентов с тяжёлыми нарушениями функции печени не установлены.
Инструкции по обращению и использованию
Внимание: не автоклавируйте иглу, входящую в комплект с препаратом!
Дотрагиваться до иглы во время её использования нельзя.
- Извлечь стеклянный корпус шприца из контурной ячейковой упаковки и убедиться в отсутствии повреждений. Разорвать внешнюю упаковку безопасной иглы (SafetyGlide). Сломать перемычку белой пластиковой крышки наконечника шприца и удалить крышку с прикреплённой резиновой заглушкой наконечника (см. Рисунок 1).
- Вращательным движением закрепить иглу на наконечнике шприца (см. Рисунок 2). Снять футляр иглы строго по её направлению, чтобы не повредить кончик иглы. Визуально оценить состояние раствора для парентерального введения на предмет отсутствия частиц и изменения цвета перед его использованием. Удалить лишние пузырьки газа из шприца.
- Медленно ввести раствор в ягодичную мышцу в течение 1–2 мин. Для удобства плоскость «скоса» кончика иглы соответствует расположению рычага на устройстве безопасности, как показано на Рисунке 3.
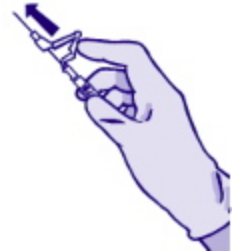
- После извлечения иглы из ягодичной мышцы незамедлительно активировать защитное устройство иглы, надавливая на рычаг с переводом его в крайнее переднее положение до тех пор, пока кончик иглы не будет полностью закрыт (см. Рисунок 4). При активации защитного механизма возможны минимальные брызги жидкости, которая может оставаться на игле после инъекции. Визуально убедиться, что рычаг переведён в крайнее положение и кончик иглы полностью закрыт. Если не удаётся активировать защитное устройство иглы, немедленно поместите иглу в стандартный контейнер для игл. Внимание: Для максимальной безопасности пользуйтесь одной рукой и выполняйте манипуляции на отдалении от себя и окружающих.
Рисунок 1.
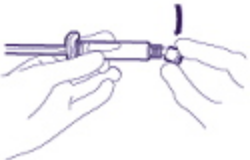
Рисунок 2.
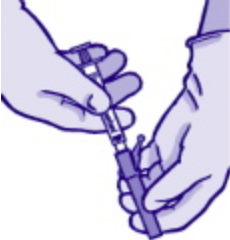
Рисунок 3.
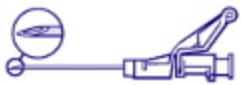
Рисунок 4.
Побочное действие
Наблюдавшиеся нежелательные реакции представлены ниже.
Определение частоты побочных реакций: очень часто (>10 %); часто (>1 — <10 %); нечасто (>0,1 — <1 %).
Со стороны системы пищеварения:
Очень часто — тошнота;
Часто — рвота, диарея, анорексия.
Со стороны сердечно-сосудистой системы:
Часто — ощущение жара («приливы»), тромбоэмболия.
Со стороны кожи и кожных придатков:
Часто — сыпь.
Местные реакции:
Очень часто — реакции в месте введения препарата, включая слабо выраженные транзиторные боль и воспаление;
Нечасто — кровотечение, гематома в месте введения.
Со стороны мочеполовой системы:
Часто — инфекции мочевыводящих путей;
Нечасто — вагинальный кандидоз, бели, вагинальные кровотечения.
Со стороны печени и желчевыводящих путей:
Очень часто — повышение активности «печёночных» ферментов (аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT), щелочной фосфатазы);
Часто — повышение концентрации билирубина;
Нечасто — печёночная недостаточность, гепатит, повышение активности гаммаглютамилтрансферазы.
Прочие:
Очень часто — астения;
Часто — головная боль, реакции повышенной чувствительности (отёки, крапивница).
Передозировка
Случаи передозировки у человека неизвестны. В исследованиях на животных при введении высоких доз фулвестранта наблюдались только эффекты, непосредственно или опосредованно связанные с антиэстрогенной активностью.
В случаях передозировки рекомендуется симптоматическая терапия.
Взаимодействие с другими лекарственными средствами
По результатам исследования клинического взаимодействия с мидазоламом фулвестрант не подавляет активность CYP ЗА4. Данные in vitro свидетельствуют, что фулвестрант не влияет на активность CYP 1A2, 2C9, 2C19 и 2D6. Возможное подавление активности CYP 2A6,2C8 и 2E1 не оценивалась.
В исследовании клинического взаимодействия с рифампицином (индуктор CYP ЗА4) и кетоконазолом (ингибитор CYP ЗA4) не обнаружено клинически значимых изменений клиренса фулвестранта. Поэтому при назначении фулвестранта в комбинации с индукторами или ингибиторами CYP ЗA4 коррекции дозы не требуется
Особые указания
Лечение препаратом Фазлодекс® должно проводиться только под наблюдением врача, имеющего опыт применения противоопухолевых препаратов.
Рекомендуется соблюдать осторожность при применении препарата Фазлодекс® пациентами с лёгким или умеренным нарушением функции печени. Рекомендуется соблюдать осторожность при использовании препарата Фазлодекс® у пациентов с тяжёлым нарушением функции почек (клиренс креатинина <30 мл/мин).
Учитывая способ применения препарата, рекомендуется соблюдать осторожность при использовании препарата Фазлодекс® у пациентов со склонностью к кровотечениям, тромбоцитопенией или у пациентов, принимающих антикоагулянты.
Тромбоэмболии у женщин с распространённым раком молочной железы наблюдаются часто. Это необходимо принимать во внимание при назначении препарата Фазлодекс® пациентам с риском тромбоэмболии.
Эффекты длительного применения фулвестранта на костную ткань не установлены. Учитывая механизм действия фулвестранта, нельзя исключить потенциальный риск остеопороза.
Фазлодекс® не должен смешиваться с другими лекарственными препаратами.
Влияние на способность управлять транспортными средствами, механизмами
Влияние препарата Фазлодекс® на способность управлять автомобилем и другими механизмами незначительно. Пациентам с симптомами астении необходимо соблюдать осторожность при управлении автомобилем или другими механизмами.
Форма выпуска
Раствор для внутримышечного введения 250 мг/5 мл.
По 5 мл в стеклянный шприц с безопасной системой введения.
По одному шприцу вместе с одной запечатанной безопасной стерильной иглой (SafetyGlide™) в контурную ячейковую упаковку из полипропилена, запечатанную полипропиленовой плёнкой. По одной контурной ячейковой упаковке вместе с инструкцией по применению в картонную пачку.
Или
по два шприца вместе с двумя запечатанными безопасными стерильными иглами (SafetyGlide™) в контурную ячейковую упаковку из полипропилена, запечатанную полипропиленовой плёнкой. По одной контурной ячейковой упаковке вместе с инструкцией по применению в картонную пачку с контролем первого вскрытия.
Хранение
При температуре от 2 до 8 °C, в защищённом от света месте.
Хранить в местах, недоступных для детей.
Срок годности
4 года.
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
Отпускают по рецепту
Производитель
Vetter Pharma-Fertigung, GmbH & Co. KG, Германия
Подробнее по теме
Ознакомьтесь с дополнительными сведениями о препарате Фазлодекс:
