ЛОПРЕССОР
LopressorТорговое наименование
ЛОПРЕССОР
Международное непатентованное наименование
Лекарственная форма
таблетки
Фармакотерапевтическая группа
Листок-вкладыш: информация для пациентов
ЛОПРЕССОР — метопролола тартрат таблетки
Основные сведения инструкции
Эти основные сведения не включают всю информацию, необходимую для безопасного и эффективного применения ЛОПРЕССОРА®. См. полную инструкцию по применению для ЛОПРЕССОР® таблетки.
ЛОПРЕССОР® (метопролола тартрат) таблетки, для перорального применения
Первоначальное одобрение в США: 1992
Показания к применению
ЛОПРЕССОР является бета-адреноблокатором, показанным для лечения гемодинамически стабильных взрослых пациентов с инфарктом миокарда, для снижения риска сердечно-сосудистой смертности. (1.1)
Дозировка и применение
Инфаркт миокарда: Рекомендуемая начальная доза составляет 50 мг перорально каждые 6 часов. Поддерживающая доза зависит от гемодинамической переносимости, см. полную инструкцию. (2.1)
Лекарственные формы и дозировки
Таблетки: 12.5 мг метопролола тартрата (3)
Противопоказания
Выраженная брадикардия: Блокада сердца более чем первой степени или синдром слабости синусового узла без кардиостимулятора. (4)
Кардиогенный шок или декомпенсированная сердечная недостаточность. (4)
Известная гиперчувствительность к компонентам препарата. (4)
Предупреждения и меры предосторожности
Резкое прекращение приёма может усугубить ишемию миокарда. (5.1)
Сердечная недостаточность: Может произойти ухудшение сердечной недостаточности. (5.2)
Бронхоспастические заболевания: Избегайте применения бета-блокаторов. (5.3)
Феохромоцитома: Начинайте терапию с альфа-блокатора. (5.4)
Обширная хирургия: Избегайте начала терапии высокими дозами метопролола у пациентов, подвергающихся некардиохирургическим операциям. Не отменяйте рутинно хроническую терапию бета-блокаторами перед операцией. (5.5, 6.1)
Диабет: Может маскировать симптомы гипогликемии. (5.6)
Тиреотоксикоз: Резкая отмена у пациентов с тиреотоксикозом может спровоцировать тиреоидный шторм. (5.7)
Заболевания периферических сосудов: Может усугублять симптомы артериальной недостаточности. (5.9)
Нежелательные реакции
Наиболее частые нежелательные реакции в условиях лечения инфаркта миокарда — гипотензия и брадикардия. (6.1)
Для сообщения о ПОДОЗРЕВАЕМЫХ НЕЖЕЛАТЕЛЬНЫХ РЕАКЦИЯХ свяжитесь с Vapdus Pharmaceuticals LLC по тел. 1-866-982-5438 или с FDA по тел. 1-800-FDA-1088 или на сайте www.fda.gov/medwatch.
Лекарственные взаимодействия
Катехоламин-истощающие препараты могут оказывать аддитивный эффект при назначении с бета-блокаторами. (7.1)
Пациенты могут не реагировать на обычные дозы эпинефрина, используемые для лечения аллергических реакций. (7.2)
Ингибиторы CYP2D6, вероятно, увеличивают концентрацию метопролола. (7.3)
Совместное применение гликозидов, клонидина, дилтиазема и верапамила с бета-блокаторами может увеличить риск брадикардии. (7.4)
Бета-блокаторы, включая метопролол, могут усугублять рикошетную гипертензию, которая может последовать после отмены клонидина. (7.4)
Применение в отдельных группах населения
Нарушение функции печени: Рассмотрите возможность начала терапии ЛОПРЕССОРОМ с низких доз и постепенно увеличивайте дозировку для оптимизации терапии, при тщательном мониторинге нежелательных явлений. (8.6)
См. раздел 17 о Информации для консультирования пациентов.
Пересмотрено: 8/2025
Содержание*
1 ПОКАЗАНИЯ И ПРИМЕНЕНИЕ
1.1 Инфаркт миокарда
2 ДОЗИРОВКА И ПРИМЕНЕНИЕ
2.1 Инфаркт миокарда
3 ЛЕКАРСТВЕННЫЕ ФОРМЫ И ДОЗИРОВКИ
4 ПРОТИВОПОКАЗАНИЯ
5 ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ
5.1 Резкое прекращение терапии
5.2 Сердечная недостаточность
5.3 Бронхоспастические заболевания
5.4 Феохромоцитома
5.5 Обширная хирургия
5.6 Гипогликемия
5.7 Тиреотоксикоз
5.8 Риск анафилактических реакций
5.9 Заболевания периферических сосудов
6 НЕЖЕЛАТЕЛЬНЫЕ РЕАКЦИИ
6.1 Опыт клинических испытаний
6.2 Опыт постмаркетингового применения
7 ЛЕКАРСТВЕННЫЕ ВЗАИМОДЕЙСТВИЯ
7.1 Катехоламин-истощающие препараты
7.2 Эпинефрин
7.3 Ингибиторы CYP2D6
7.4 Отрицательные хронотропы
8 ПРИМЕНЕНИЕ В ОТДЕЛЬНЫХ ГРУППАХ НАСЕЛЕНИЯ
8.1 Беременность
8.2 Лактация
8.3 Женщины и мужчины репродуктивного потенциала
8.4 Применение в педиатрии
8.5 Применение у пожилых пациентов
8.6 Нарушение функции печени
8.7 Нарушение функции почек
10 ПЕРЕДОЗИРОВКА
11 ОПИСАНИЕ
12 КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
12.1 Механизм действия
12.2 Фармакодинамика
12.3 Фармакокинетика
12.5 Фармакогеномика
13 ДОКЛИНИЧЕСКАЯ ТОКСИКОЛОГИЯ
13.1 Канцерогенность, мутагенность, нарушение фертильности
14 КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
14.1 Инфаркт миокарда
15 ФОРМА ВЫПУСКА/ХРАНЕНИЕ И ОБРАЩЕНИЕ
16 ИНФОРМАЦИЯ ДЛЯ КОНСУЛЬТИРОВАНИЯ ПАЦИЕНТОВ
* Разделы или подразделы, опущенные в полной инструкции по применению, не указаны.
ПОЛНАЯ ИНСТРУКЦИЯ ПО ПРИМЕНЕНИЮ
1. ПОКАЗАНИЯ И ПРИМЕНЕНИЕ
1.1 Инфаркт миокарда
ЛОПРЕССОР показан для лечения гемодинамически стабильных взрослых пациентов с инфарктом миокарда (ИМ) для снижения сердечно-сосудистой смертности.
2. ДОЗИРОВКА И ПРИМЕНЕНИЕ
2.1 Инфаркт миокарда
Рекомендуемая начальная доза для гемодинамически стабильных пациентов составляет 50 мг перорально каждые 6 часов. В случае непереносимости уменьшите начальную дозу до 25 мг перорально каждые 6 часов и вводите в течение 48 часов. Титруйте дозу на основе переносимости и гемодинамических параметров (т.е. частота сердечных сокращений, артериальное давление). ЛОПРЕССОР предпочтительно принимать во время или после еды. Максимальная суточная поддерживающая доза составляет 100 мг перорально два раза в день.
3. ЛЕКАРСТВЕННЫЕ ФОРМЫ И ДОЗИРОВКИ
ЛОПРЕССОР поставляется в виде таблетки 12.5 мг, которая имеет розовый цвет, плёночную оболочку, круглую, двояковыпуклую форму, с тиснением "'E" на одной стороне и гладкая с другой стороны.
4. ПРОТИВОПОКАЗАНИЯ
ЛОПРЕССОР противопоказан при выраженной брадикардии, атриовентрикулярной блокаде второй или третьей степени, кардиогенном шоке, систолическом артериальном давлении <100 мм рт.ст., декомпенсированной сердечной недостаточности, синдроме слабости синусового узла (если не установлен постоянный кардиостимулятор), и у пациентов с гиперчувствительностью к любому компоненту этого продукта.
5. ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ
5.1 Резкое прекращение терапии
После резкого прекращения терапии некоторыми бета-блокаторами наблюдались обострения стенокардии и, в некоторых случаях, инфаркт миокарда. При прекращении длительно назначаемого ЛОПРЕССОРА постепенно уменьшайте дозу в течение периода от 1 до 2 недель и контролируйте пациента. Предупредите пациентов не прерывать терапию без совета врача.
5.2 Сердечная недостаточность
Ухудшение сердечной недостаточности может произойти во время титрования дозы ЛОПРЕССОРА вверх. Если такие симптомы возникают, увеличьте диуретики и восстановите клиническую стабильность перед увеличением дозы ЛОПРЕССОРА [см. Дозировка и применение (2)]. Может быть необходимо снизить дозу ЛОПРЕССОРА или временно прекратить его. Такие эпизоды не препятствуют последующему успешному титрованию ЛОПРЕССОРА.
5.3 Бронхоспастические заболевания
Пациентам с бронхоспастическими заболеваниями, как правило, не следует назначать бета-блокаторы, включая ЛОПРЕССОР. Однако, благодаря своей относительной бета1-кардиоселективности, ЛОПРЕССОР может использоваться у пациентов с бронхоспастическими заболеваниями, которые не отвечают на другие антигипертензивные препараты или не переносят их. Поскольку бета1-селективность не является абсолютной, используйте минимально возможную дозу ЛОПРЕССОРА. Бронходилататоры, включая бета2-агонисты, должны быть легко доступны или назначаться одновременно [см. Дозировка и применение (2)].
5.4 Феохромоцитома
Если ЛОПРЕССОР используется в условиях феохромоцитомы, его следует назначать в комбинации с альфа-блокатором и только после начала приёма альфа-блокатора. Введение только бета-блокаторов в условиях феохромоцитомы ассоциировалось с парадоксальным повышением артериального давления из-за ослабления бета-опосредованной вазодилатации в скелетных мышцах.
5.5 Обширная хирургия
Избегайте начала терапии высокими дозами бета-блокаторов у пациентов, подвергающихся некардиохирургическим операциям, поскольку такое применение у пациентов с факторами сердечно-сосудистого риска ассоциировалось с брадикардией, гипотензией, инсультом и смертью.
Хроническую терапию бета-блокаторами не следует рутинно отменять перед обширной операцией, однако, нарушенная способность сердца реагировать на рефлекторные адренергические стимулы может увеличивать риски общей анестезии и хирургических процедур.
5.6 Гипогликемия
Бета-блокаторы могут предотвращать ранние предупреждающие признаки гипогликемии, такие как тахикардия, и увеличивать риск тяжёлой или пролонгированной гипогликемии в любое время во время лечения, особенно у пациентов с сахарным диабетом или детей и пациентов, которые голодают (т.е. операция, нерегулярное питание или рвота). Если возникает тяжёлая гипогликемия, пациенты должны быть проинструктированы обращаться за неотложной помощью.
5.7 Тиреотоксикоз
Бета-адренергическая блокада может маскировать определённые клинические признаки гипертиреоза, такие как тахикардия. Резкая отмена бета-блокады может спровоцировать тиреоидный шторм.
5.8 Риск анафилактических реакций
При приёме бета-блокаторов пациенты с историей тяжёлых анафилактических реакций на различные аллергены могут быть более реактивными при повторном воздействии, будь то случайном, диагностическом или терапевтическом. Такие пациенты могут не реагировать на обычные дозы эпинефрина, используемые для лечения аллергических реакций.
5.9 Заболевания периферических сосудов
Бета-блокаторы могут провоцировать или усугублять симптомы артериальной недостаточности у пациентов с заболеваниями периферических сосудов.
6. НЕЖЕЛАТЕЛЬНЫЕ РЕАКЦИИ
Следующие нежелательные реакции описаны в других разделах инструкции:
- Ухудшение ишемии при резком прекращении приёма [см. Предупреждения и меры предосторожности (5)]
- Ухудшение сердечной недостаточности [см. Предупреждения и меры предосторожности (5)].
- Ухудшение атриовентрикулярной (AV) блокады [см. Противопоказания (4)].
6.1 Опыт клинических испытаний
Поскольку клинические испытания проводятся в широко варьирующихся условиях, частоты нежелательных реакций, наблюдаемые в клинических испытаниях одного препарата, нельзя напрямую сравнивать с частотами в клинических испытаниях другого препарата и они могут не отражать частоты, наблюдаемые на практике.
Инфаркт миокарда
В рандомизированном сравнении ЛОПРЕССОРА и плацебо в условиях острого ИМ [см. Клинические исследования 14.1] были зарегистрированы следующие нежелательные реакции:
| Нежелательная реакция | ЛОПРЕССОР N=698 % | Плацебо N=697 % |
|---|---|---|
| Гипотензия (систолическое АД < 90 мм рт.ст.) | 27.4 % | 23.2 % |
| Брадикардия (частота сердечных сокращений < 40 уд/мин) | 15.9 % | 6.7 % |
| АВ-блокада второй или третьей степени | 4.7 % | 4.7 % |
| АВ-блокада первой степени (P-R ≥ 0.26 сек) | 5.3 % | 1.9 % |
| Сердечная недостаточность | 27.5 % | 29.6 % |
6.2 Опыт постмаркетингового применения
Следующие нежелательные реакции были зарегистрированы в ходе применения ЛОПРЕССОРА после одобрения. Поскольку эти реакции сообщаются добровольно из популяции неопределённого размера, не всегда возможно надёжно оценить их частоту или установить причинно-следственную связь с приёмом препарата.
Центральная нервная система: Обратимая психическая депрессия, прогрессирующая до кататонии; острый обратимый синдром, характеризующийся дезориентацией во времени и месте, кратковременной потерей памяти, эмоциональной лабильностью, слегка затуманенным сенсориумом и снижением когнитивной деятельности.
Сердечно-сосудистая система: Ухудшение AV-блокады [см. Противопоказания (4)].
Гематологические: Агранулоцитоз, нетромбоцитопеническая пурпура и тромбоцитопеническая пурпура.
Реакции гиперчувствительности: Лихорадка в сочетании с ломотой и болью в горле, ларингоспазм и респираторный дистресс.
Лабораторные показатели:
Повышение триглицеридов в крови, повышение трансаминаз и снижение липопротеинов высокой плотности (ЛПВП).
7. ЛЕКАРСТВЕННЫЕ ВЗАИМОДЕЙСТВИЯ
7.1 Катехоламин-истощающие препараты
Наблюдайте за пациентами, получающими ЛОПРЕССОР плюс катехоламин-истощающий препарат, на предмет признаков гипотензии или выраженной брадикардии, которые могут вызывать головокружение, синкопе или ортостатическую гипотензию. Катехоламин-истощающие препараты (например, резерпин, ингибиторы моноаминоксидазы (МАО)) могут оказывать аддитивный эффект при назначении с бета-блокаторами.
7.2 Эпинефрин
Кардиостимулирующие и бронхорасширяющие эффекты эпинефрина антагонизируются бета-адреноблокаторами, такими как метопролол. Могут потребоваться более высокие дозы эпинефрина для пациентов, принимающих метопролол.
7.3 Ингибиторы CYP2D6
Тщательно контролируйте пациентов, когда комбинированное применение ингибитора CYP2D6 и метопролола невозможно избежать. Было показано, что препараты, являющиеся сильными ингибиторами CYP2D6, такие как хинидин, флуоксетин, пароксетин и пропафенон, удваивают концентрации метопролола. Хотя нет информации об ингибиторах средней или слабой силы, они также могут увеличивать концентрацию метопролола. Увеличение плазменной концентрации уменьшает бета1-кардиоселективность метопролола [см. Клиническая фармакология (12.3)].
7.4 Отрицательные хронотропы
Если клонидин и метопролол назначаются совместно, отмените бета-блокатор за несколько дней до постепенной отмены клонидина, потому что метопролол может усугубить рикошетную гипертензию, которая может последовать после отмены клонидина. Если заменяете клонидин на метопролол, отложите введение метопролола на несколько дней после прекращения приёма клонидина.
Гликозиды наперстянки, клонидин, дилтиазем и верапамил замедляют атриовентрикулярную проводимость и уменьшают частоту сердечных сокращений. Совместное применение с бета-блокаторами может увеличить риск брадикардии.
8. ПРИМЕНЕНИЕ В ОТДЕЛЬНЫХ ГРУППАХ НАСЕЛЕНИЯ
8.1 Беременность
Резюме риска
Имеющиеся данные опубликованных обсервационных исследований не продемонстрировали связи неблагоприятных исходов развития с применением метопролола матерью во время беременности (см. Данные). Нелеченный инфаркт миокарда во время беременности может привести к неблагоприятным исходам для матери и плода (см. Клинические соображения). В исследованиях репродукции у животных было показано, что метопролол увеличивает потери после имплантации и снижает выживаемость новорождённых у крыс при пероральных дозах 500 мг/кг/день, что примерно в 11 раз превышает суточную дозу 450 мг у пациента весом 60 кг в пересчёте на мг/м2.
Все беременности имеют фоновый риск врождённых дефектов, потери или других неблагоприятных исходов. Оценочный фоновый риск основных врожденных дефектов и выкидыша для указанной популяции неизвестен. В общей популяции США оценочный фоновый риск основных врождённых дефектов и выкидыша в клинически распознаваемых беременностях составляет от 2 до 4 % и от 15 до 20 % соответственно.
Клинические соображения
Нежелательные реакции у плода/новорождённого
Метопролол проникает через плаценту. Новорождённые, рождённые матерями, которые получают метопролол во время беременности, могут быть подвержены риску гипотензии, гипогликемии, брадикардии и угнетения дыхания. Наблюдайте за новорождёнными и принимайте соответствующие меры.
Данные
Данные по людям
Данные опубликованных обсервационных исследований не продемонстрировали связи основных врождённых мальформаций с применением метопролола во время беременности. В опубликованной литературе сообщались противоречивые данные о задержке внутриутробного развития, преждевременных родах и перинатальной смертности при применении метопролола матерью во время беременности; однако эти исследования имеют методологические ограничения, затрудняющие интерпретацию. Методологические ограничения включают ретроспективный дизайн, сопутствующее применение других лекарственных препаратов и другие нескорректированные вмешивающиеся факторы, которые могут объяснить результаты исследований, включая основное заболевание у матери. Эти обсервационные исследования не могут окончательно установить или исключить какой-либо риск, связанный с препаратом, во время беременности.
Данные по животным
Было показано, что метопролол увеличивает потери после имплантации и снижает выживаемость новорождённых у крыс при пероральных дозах 500 мг/кг/день, т.е. в 11 раз, в пересчёте на мг/м2, по сравнению с суточной дозой 450 мг у пациента весом 60 кг.
Не наблюдалось аномалий плода, когда беременные крысы получали метопролол перорально до дозы 200 мг/кг/день, т.е. в 4 раза больше суточной дозы 400 мг у пациента весом 60 кг.
8.2 Лактация
Резюме риска
Ограниченные доступные данные из опубликованной литературы сообщают, что метопролол присутствует в грудном молоке. Расчётная суточная доза метопролола, получаемая младенцем из грудного молока, составляет от 0,05 мг до менее 1 мг. Расчётная относительная детская доза составляла от 0,5 % до 2 % от скорректированной на вес матери дозы (см. Данные). Не было выявлено нежелательных реакций метопролола на грудного ребёнка. Нет информации относительно влияния метопролола на выработку молока.
Клинические соображения
Мониторинг нежелательных реакций
Для кормящей женщины, которая является медленным метаболизатором метопролола, контролируйте грудного ребёнка на предмет брадикардии и других симптомов бета-блокады, таких как сухость во рту, коже или глазах, диарея или запор. В отчёте о 6 матерях, принимающих метопролол, ни одна не сообщила о неблагоприятных эффектах у своего грудного ребёнка.
Данные
Ограниченные опубликованные случаи оценивают суточную дозу метопролола, получаемую младенцем из грудного молока, в диапазоне от 0,05 мг до менее 1 мг.
У 2 женщин, принимавших неопределённое количество метопролола, были взяты образцы молока после одной дозы метопролола. Сообщается, что расчётное количество метопролола и альфа-гидроксиметопролола в грудном молоке составляет менее 2 % от скорректированной на вес матери дозы.
В небольшом исследовании грудное молоко собирали каждые 2–3 часа в течение одного интервала дозирования у трех матерей (не менее 3 месяцев после родов), которые принимали метопролол в неопределённом количестве. Среднее количество метопролола, присутствующего в грудном молоке, составляло 71,5 мкг/день (диапазон от 17,0 мкг до 158,7 мкг). Средняя относительная детская доза составляла 0,5 % от скорректированной на вес матери дозы.
8.3 Женщины и мужчины репродуктивного потенциала
Резюме риска
На основании опубликованной литературы, бета-блокаторы (включая метопролол) могут вызывать эректильную дисфункцию и ингибировать подвижность сперматозоидов. В исследованиях фертильности у животных метопролол ассоциировался с обратимыми неблагоприятными эффектами на сперматогенез, начиная с пероральной дозы 3,5 мг/кг у крыс, что соответствовало бы дозе 34 мг/день у людей в пересчёте на мг/м2 эквивалент, хотя другие исследования не показали влияния метопролола на репродуктивную функцию у самцов крыс.
Не было обнаружено свидетельств нарушения фертильности из-за метопролола у крыс [см. Доклиническая токсикология (13.1)].
8.4 Применение в педиатрии
Безопасность и эффективность ЛОПРЕССОРА не установлены у педиатрических пациентов.
8.5 Применение у пожилых пациентов
В мировых клинических испытаниях ЛОПРЕССОРА при инфаркте миокарда, где приблизительно 478 пациентов были старше 65 лет (0 старше 75 лет), не было обнаружено возрастных различий в безопасности и эффективности. Другой сообщённый клинический опыт при инфаркте миокарда не выявил различий в ответе между пожилыми и более молодыми пациентами.
В целом, используйте низкую начальную дозу у пожилых пациентов, учитывая их большую частоту снижения функции печени, почек или сердца, а также сопутствующих заболеваний или другой лекарственной терапии.
8.6 Нарушение функции печени
Не проводилось исследований ЛОПРЕССОРА у пациентов с нарушением функции печени. ЛОПРЕССОР метаболизируется печенью, уровни метопролола в крови, вероятно, будут существенно увеличиваться при плохой функции печени. Поэтому начинайте терапию с доз, меньших, чем рекомендуемые; и увеличивайте дозы постепенно у пациентов с нарушенной функцией печени.
8.7 Нарушение функции почек
Системная доступность и период полувыведения метопролола у пациентов с почечной недостаточностью не отличаются клинически значимо от таковых у нормальных субъектов. Снижение дозировки не требуется у пациентов с почечной недостаточностью [см. Клиническая фармакология (12.3)].
10. ПЕРЕДОЗИРОВКА
Признаки и симптомы — Передозировка ЛОПРЕССОРА может привести к выраженной брадикардии, гипотензии и кардиогенному шоку. Клиническая картина также может включать АВ-блокаду, сердечную недостаточность, бронхоспазм, гипоксию, нарушение сознания/кому, тошноту и рвоту.
Лечение – Рассмотрите возможность лечения пациента в условиях интенсивной терапии. Пациенты с инфарктом миокарда или сердечной недостаточностью могут быть склонны к значительной гемодинамической нестабильности. Передозировка бета-блокатором может привести к значительной резистентности к реанимации с помощью адренергических средств, включая бета-агонисты. На основе фармакологических действий метопролола применяйте следующие меры.
Гемодиализ вряд ли внесёт полезный вклад в элиминацию метопролола [см. Клиническая фармакология (12.3)].
Брадикардия: Оцените необходимость в атропине, адренергически-стимулирующих препаратах или кардиостимуляторе для лечения брадикардии и нарушений проводимости.
Гипотензия: Лечите основную брадикардию. Рассмотрите внутривенную инфузию вазопрессоров, таких как допамин или норадреналин.
Сердечная недостаточность и шок: Могут лечиться, когда это уместно, с помощью соответствующего восполнения объёма, введения глюкагона (при необходимости, с последующей внутривенной инфузией глюкагона), внутривенного введения адренергических препаратов, таких как добутамин, с добавлением агонистов α1-рецепторов при наличии вазодилатации.
Бронхоспазм: Обычно может быть купирован бронходилататорами.
11. ОПИСАНИЕ
Таблетки ЛОПРЕССОР содержат метопролола тартрат, бета-адреноблокатор. Метопролола тартрат представляет собой (+-)-1-(Изопропиламино)-3-[п-(2-метоксиэтил) фенокси]-2-пропанол L-(+)-тартрат (2:1) соль, и его структурная формула:
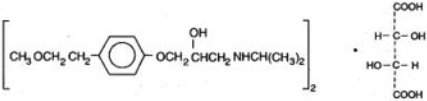
Метопролола тартрат ФС представляет собой белый, практически без запаха, кристаллический порошок с молекулярной массой 684.82 г/моль. Он очень растворим в воде; свободно растворим в хлористом метилене, в хлороформе и в спирте; слегка растворим в ацетоне; и нерастворим в эфире.
ЛОПРЕССОР доступен в виде таблеток 12,5 мг для перорального применения, содержащих 12,5 мг метопролола тартрата (эквивалентно 9,76 мг метопролола).
Неактивные ингредиенты: Таблетки содержат коллоидный диоксид кремния, лактозы моногидрат, стеарат магния, микрокристаллическую целлюлозу, натрия крахмала гликолят. Плёночная оболочка содержит D&C Red 30, гипромеллозу, полиэтиленгликоль, тальк и диоксид титана.
12. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
12.1 Механизм действия
Метопролол является селективным бета1-адренергическим рецепторным блокатором. Это предпочтительное действие не является абсолютным, однако, и при более высоких плазменных концентрациях метопролол также ингибирует бета2-адренорецепторы, в основном расположенные в бронхиальной и сосудистой мускулатуре.
Метопролол не обладает внутренней симпатомиметической активностью, а мембраностабилизирующая активность обнаруживается только при плазменных концентрациях, намного превышающих необходимые для бета-блокады. Эксперименты на животных и людях указывают на то, что метопролол замедляет синусовый ритм и уменьшает АВ-проводимость.
Относительная бета1-селективность метопролола была подтверждена следующим: (1) У здоровых субъектов метопролол не способен обращать бета2-опосредованные вазодилатирующие эффекты эпинефрина. Это контрастирует с эффектом неселективных бета-блокаторов, которые полностью обращают вазодилатирующие эффекты эпинефрина. (2) У пациентов с астмой метопролол уменьшает ОФВ1 и ФЖЕЛ значительно меньше, чем неселективный бета-блокатор, пропранолол, в эквивалентных бета1-рецептор блокирующих дозах.
12.2 Фармакодинамика
Исследования клинической фармакологии подтвердили бета-блокирующую активность метопролола у людей, как показано (1) снижением частоты сердечных сокращений и сердечного выброса в покое и при нагрузке, (2) снижением систолического артериального давления при нагрузке, (3) ингибированием индуцированной изопротеренолом тахикардии и (4) снижением рефлекторной ортостатической тахикардии.
Зависимость между уровнями метопролола в плазме и снижением частоты сердечных сокращений при нагрузке не зависит от фармацевтической формы. Бета1-блокирующие эффекты в диапазоне 30–80 % от максимального эффекта (примерно от 8 до 23 % снижения частоты сердечных сокращений при нагрузке) соответствуют плазменным концентрациям метопролола от 30 до 540 нмоль/л. Относительная бета1-селективность метопролола уменьшается, а блокада бета2-адренорецепторов увеличивается при плазменных концентрациях выше 300 нмоль/л.
12.3 Фармакокинетика
Всасывание: Расчётная пероральная биодоступность метопролола немедленного высвобождения составляет около 50 % из-за пресистемного метаболизма, который является насыщаемым, что приводит к непропорциональному увеличению экспозиции с увеличением дозы.
Распределение: Метопролол широко распределяется с заявленным объёмом распределения от 3,2 до 5,6 л/кг. Около 10 % метопролола в плазме связано с сывороточным альбумином. Известно, что метопролол проникает через плаценту и обнаруживается в грудном молоке. Также известно, что метопролол проникает через гематоэнцефалический барьер после перорального введения, и сообщалось о концентрациях в спинномозговой жидкости (ЦСЖ), близких к наблюдаемым в плазме. Метопролол не является значимым субстратом P-гликопротеина.
Элиминация:
Элиминация ЛОПРЕССОР в основном происходит путём биотрансформации в печени. Средний период полувыведения метопролола составляет от 3 до 4 часов; у медленных метаболизаторов CYP2D6 период полувыведения может составлять от 7 до 9 часов.
Метаболизм: ЛОПРЕССОР в основном метаболизируется CYP2D6. Метопролол представляет собой рацемическую смесь R- и S- энантиомеров, и при пероральном введении он проявляет стереоселективный метаболизм, который зависит от фенотипа окисления. CYP2D6 отсутствует (медленные метаболизаторы) примерно у 8 % европеоидов и около 2 % большинства других популяций. Медленные метаболизаторы CYP2D6 проявляют в несколько раз более высокие плазменные концентрации метопролола тартрата, чем быстрые метаболизаторы с нормальной активностью CYP2D6, тем самым уменьшая кардиоселективность метопролола тартрата.
Выведение: Приблизительно 95 % дозы может быть восстановлено в моче. У большинства испытуемых (быстрых метаболизаторов) менее 5 % пероральной дозы выводится почками в неизмененном виде, а остальное выводится почками в виде метаболитов, которые, по-видимому, не обладают бета-блокирующей активностью. Почечный клиренс стереоизомеров не проявляет стереоселективности при почечной экскреции.
Конкретные популяции
Пожилые пациенты: У пожилого населения могут наблюдаться несколько более высокие плазменные концентрации метопролола как совокупный результат сниженного метаболизма препарата у пожилых людей и сниженного печёночного кровотока. Однако это увеличение не является клинически значимым или терапевтически релевантным.
Пациенты с нарушением функции почек: Системная доступность и период полувыведения ЛОПРЕССОР у пациентов с почечной недостаточностью не отличаются клинически значимо от таковых у нормальных субъектов.
Пациенты с нарушением функции печени: Поскольку препарат в основном элиминируется путём печёночного метаболизма, нарушение функции печени может влиять на фармакокинетику метопролола.
Лекарственные взаимодействия:
Метопролол метаболизируется преимущественно CYP2D6. У здоровых субъектов с фенотипом быстрого метаболизатора CYP2D6 совместное введение хинидина 100 мг, мощного ингибитора CYP2D6, и метопролола немедленного высвобождения 200 мг утроило концентрацию S-метопролола и удвоило период полувыведения метопролола. У четырех пациентов с сердечно-сосудистыми заболеваниями совместное введение пропафенона 150 мг три раза в день с метопрололом немедленного высвобождения 50 мг три раза в день увеличивало равновесную концентрацию метопролола в 2–5 раз по сравнению с одним метопрололом. Быстрые метаболизаторы, которые одновременно используют ингибирующие CYP2D6 препараты, будут иметь повышенные (в несколько раз) уровни метопролола в крови, уменьшая кардиоселективность метопролола [см. Лекарственные взаимодействия (7.2)].
12.5 Фармакогеномика
CYP2D6 отсутствует примерно у 8 % европеоидов (медленные метаболизаторы) и около 2 % большинства других популяций. CYP2D6 может ингибироваться несколькими препаратами. Медленные метаболизаторы CYP2D6 будут иметь повышенные (в несколько раз) уровни метопролола в крови, уменьшая кардиоселективность метопролола.
13. ДОКЛИНИЧЕСКАЯ ТОКСИКОЛОГИЯ
13.1 Канцерогенность, мутагенность, нарушение фертильности
Долгосрочные исследования на животных проводились для оценки канцерогенного потенциала метопролола тартрата. В 2-летних исследованиях на крысах при трех пероральных уровнях доз до 800 мг/кг/день (в 19 раз, в пересчёте на мг/м2, суточной дозы 400 мг для пациента весом 60 кг) не было увеличения развития спонтанно возникающих доброкачественных или злокачественных новообразований любого типа. Единственными гистологическими изменениями, которые, по-видимому, были связаны с препаратом, были увеличение частоты обычно лёгкого фокального накопления пенистых макрофагов в лёгочных альвеолах и небольшое увеличение гиперплазии желчных протоков. В 21-месячном исследовании на швейцарских белых мышах при трёх пероральных уровнях доз до 750 мг/кг/день (в 9 раз, в пересчете на мг/м2, суточной дозы 400 мг для пациента весом 60 кг) доброкачественные опухоли лёгких (мелкие аденомы) возникали чаще у самок мышей, получавших самую высокую дозу, чем у нелеченных контрольных животных. Не было увеличения злокачественных или общих (доброкачественных плюс злокачественных) опухолей лёгких, ни в общей частоте опухолей или злокачественных опухолей. Это 21-месячное исследование было повторено на мышах CD-1, и не наблюдалось статистически или биологически значимых различий между обработанными и контрольными мышами любого пола для любого типа опухоли.
Все тесты на генотоксичность, проведённые на метопролола тартрате (доминантный летальный тест на мышах, исследования хромосом в соматических клетках, тест на мутагенность Salmonella/микросомы млекопитающих и тест на аномалии ядра в соматических интерфазных ядрах) и метопролола сукцинате (тест на мутагенность Salmonella/микросомы млекопитающих) были отрицательными.
Не было обнаружено свидетельств нарушения фертильности из-за метопролола тартрата в исследовании, проведённом на крысах в дозах до 55,5 раз, в пересчёте на мг/м2, суточной дозы 450 мг у пациента весом 60 кг.
14. КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
14.1 Инфаркт миокарда
Исследование, поддерживающее одобрение метопролола после инфаркта миокарда для снижения сердечно-сосудистой смертности, проводилось до эры реперфузии. В этом двойном слепом, плацебо-контролируемом исследовании 1395 пациентов с подозрением на острый инфаркт миокарда были рандомизированы на ЛОПРЕССОР или плацебо. ЛОПРЕССОР снизил 3-месячную сердечно-сосудистую смертность на 36 %.
Пациенты были рандомизированы и лечились как можно скорее после поступления в больницу, как только их клиническое состояние стабилизировалось и их гемодинамический статус был тщательно оценён. Субъекты были не приемлемы, если у них была гипотензия, брадикардия, периферические признаки шока и/или более чем минимальные базальные хрипы как признаки застойной сердечной недостаточности. Начальное лечение состояло из внутривенного введения с последующим пероральным приёмом ЛОПРЕССОРА или плацебо, проводимого в отделении коронарной помощи или аналогичном отделении. Поддерживающая терапия ЛОПРЕССОРОМ или плацебо продолжалась в течение 3 месяцев. Медианная задержка от начала симптомов до начала терапии составила 8 часов как в группе ЛОПРЕССОРА, так и в группе плацебо. Среди пациентов, получавших ЛОПРЕССОР, наблюдалось сопоставимое снижение 3-месячной сердечно-сосудистой смертности у тех, кого лечили рано (≤ 8 часов), и тех, у кого лечение было начато позже. Значительное снижение частоты фибрилляции желудочков и боли в груди после начальной внутривенной терапии также наблюдалось с ЛОПРЕССОРОМ и не зависело от интервала между началом симптомов и началом терапии.
16. ФОРМА ВЫПУСКА/ХРАНЕНИЕ И ОБРАЩЕНИЕ
ЛОПРЕССОР (метопролола тартрат) таблетки
Таблетки 12.5 мг — розовые, покрытые плёночной оболочкой, круглые, двояковыпуклые таблетки с тиснением “E” на одной стороне и гладкие с другой стороны. Они доступны следующим образом:
Флаконы по 30 ...... NDC 30698-460-03
Флаконы по 1,000 ...... NDC 30698-460-10
Хранение:
Хранить при температуре от 20°C до 25°C (от 68°F до 77°F). [См. USP Контролируемая комнатная температура.]
Защищать от влаги.
Диспенсировать в плотном, светонепроницаемом контейнере, как определено в USP, с использованием крышки, устойчивой к вскрытию детьми.
17. ИНФОРМАЦИЯ ДЛЯ КОНСУЛЬТИРОВАНИЯ ПАЦИЕНТОВ
Посоветуйте пациентам принимать ЛОПРЕССОР регулярно и непрерывно, как направлено, предпочтительно во время или сразу после еды. Если доза пропущена, пациент должен принять только следующую запланированную дозу (без удвоения). Пациенты не должны прерывать или прекращать приём ЛОПРЕССОРА без консультации с врачом.
Посоветуйте пациентам (1) избегать вождения автомобилей и работы с механизмами или выполнения других задач, требующих бдительности, до тех пор пока не определена реакция пациента на терапию ЛОПРЕССОРОМ; (2) связаться с врачом, если возникают любые затруднения дыхания; (3) проинформировать врача или стоматолога перед любым видом операции о том, что он или она принимает ЛОПРЕССОР.
Информируйте пациентов или лиц, осуществляющих уход, о риске гипогликемии, когда ЛОПРЕССОР назначается пациентам, которые голодают или у которых рвота. Инструктируйте пациентов или лиц, осуществляющих уход, как контролировать признаки гипогликемии [см. Предупреждения и меры предосторожности (5.6)].
Изготовлено для и распространяется:
Validus Pharmaceuticals LLC
Parsippany, NJ 07054, USA
info@validuspharma.com
www.validuspharma.com
▼ Лекарственный препарат в настоящий момент не зарегистрирован в Российской Федерации. |
Форма выпуска
таблетки
Условия отпуска из аптек
Отпускают по рецепту
