Бинокрит®
, растворРегистрационный номер
Торговое наименование
Международное непатентованное наименование
Лекарственная форма
раствор для внутривенного и подкожного введения
Состав
| Раствор для внутривенного и подкожного введения 16,8 мкг/мл | ||
| Название вещества | Количество / шприц (1 доза) | |
| 1000 МЕ | 2000 МЕ | |
| Активное вещество: | ||
| 1000 МЕ (8,4 мкг) 1 | 2000 МЕ (16,8 мкг)1 | |
| Вспомогательные вещества: | ||
| натрия дигидрофосфата дигидрат | 0,7 мг | 1,4 мг |
| натрия гидрофосфата дигидрат | 1,42 мг | 2,84 мг |
| 2,19 мг | 4,38 мг | |
| 2,5 мг | 5,0 мг | |
| 0,15 мг | 0,3 мг | |
| 0,035 мг2 | 0,070 мг2 | |
| 0,035 мг2 | 0,070 мг2 | |
| до 0,5 мл | до 1,0 мл | |
|
Раствор для внутривенного и подкожного введения 84 мкг/мл | ||||
Название вещества |
Количество / шприц (1 доза) | |||
| 3000 МЕ | 4000 МЕ | 5000 МЕ | ||
| Активное вещество: | ||||
| 3000 МЕ (25,2 мкг)1 | 4000 МЕ (33,6 мкг)1 | 5000 МЕ (42,0 мкг)1 | ||
| Вспомогательные вещества: | ||||
| натрия дигидрофосфата дигидрат | 0,42 мг | 0,56 мг | 0,7 мг | |
| натрия гидрофосфата дигидрат | 0,852 мг | 1,136 мг | 1,42 мг | |
| 1,314 мг | 1,752 мг | 2,19 мг | ||
| 1,5 мг | 2,0 мг | 2,5 мг | ||
| 0,09 мг | 0,12 мг | 0,15 мг | ||
| 0,021 мг2 | 0,028 мг2 | 0,035 мг2 | ||
| 0,021 мг2 | 0,028 мг2 | 0,035 мг2 | ||
| до 0,3 мл | до 0,4 мл | до 0,5 мл | ||
| Название вещества | Количество / шприц (1 доза) | |||
| 6000 МЕ | 8000 МЕ | 10000 МЕ | ||
| Активное вещество: | ||||
| 6000 МЕ (50,4 мкг)1 | 8000 МЕ (67,2 мкг)1 | 10000 МЕ (84,0 мкг)1 | ||
| Вспомогательные вещества: | ||||
| натрия дигидрофосфата дигидрат | 0,84 мг | 1,12 мг | 1,4 мг | |
| натрия гидрофосфата дигидрат | 1,704 мг | 2,272 мг | 2,84 мг | |
| 2,628 мг | 3,504 мг | 4,38 мг | ||
| 3,0 мг | 4,0 мг | 5,0 мг | ||
| 0,18 мг | 0,24 мг | 0,3 мг | ||
| 0,042 мг2 | 0,056 мг2 | 0,070 мг2 | ||
| 0,042 мг2 | 0,056 мг2 | 0,070 мг2 | ||
| до 0,6 мл | до 0,8 мл | до 1,0 мл | ||
| Раствор для внутривенного и подкожного введения 336 мкг/мл | |||
| Название вещества | Количество / шприц (1 доза) | ||
| 20000 МЕ | 30000 МЕ | 40000 МЕ | |
| Активное вещество: | |||
| 20000 МЕ (168 мкг)1 | 30000 МЕ (252 мкг)1 | 40000 МЕ (336 мкг)1 | |
| Вспомогательные вещества: | |||
| натрия дигидрофосфата дигидрат | 0,7 мг | 1,05 мг | 1,4 мг |
| натрия гидрофосфата дигидрат | 1,42 мг | 2,13 мг | 2,84 мг |
| 2,19 мг | 3,29 мг | 4,38 мг | |
| 2,5 мг | 3,75 мг | 5,0 мг | |
| 0,15 мг | 0,23 мг | 0,3 мг | |
| 0,035 мг2 | 0,053 мг2 | 0,070 мг2 | |
| 0,035 мг2 | 0,053 мг2 | 0,070 мг2 | |
| до 0,5 мл | до 0,75 мл | до 1,0 мл | |
1 1 мг эпоэтина альфа соответствует 120000 МЕ.
2 Добавляется в случае необходимости регулирования pH раствора (максимальное количество, соответствующее 0,1 М раствору вещества).
Описание
Прозрачный бесцветный раствор.
Фармакотерапевтическая группа
Код АТХ
Фармакологические свойства
Фармакодинамика
Эритропоэтин представляет собой гликопротеин, который стимулирует эритропоэз, активирует митоз и созревание эритроцитов из клеток-предшественников эритроцитарного ряда. Молекулярная масса эритропоэтина составляет около 32000–40000 дальтон. Белковая фракция составляет около 58 % молекулярной массы и включает 165 аминокислот. Четыре углеводородных цепи связаны с белком тремя N-гликозидными связями и одной О-гликозидной связью. Эпоэтин альфа, получаемый с использованием генно-инженерной технологии, представляет собой очищенный гликопротеин, по аминокислотному и углеводному составу он идентичен эритропоэтину человека, выделяемому из мочи у пациентов при анемии.
Бинокрит® имеет максимально высокую степень очистки в соответствии с современными технологическими возможностями. В частности, при количественном анализе активного вещества препарата Бинокрит® не определяются даже следовые количества клеточных линий, на которых осуществляется производство препарата. Биологическая активность эпоэтина альфа подтверждена в эксперименте in vivo (исследования проводили на здоровых крысах и крысах с анемией, а также на мышах с полицитемией). После введения эпоэтина альфа число эритроцитов, ретикулоцитов, концентрация гемоглобина и скорость поглощения 59Fе возрастают.
В исследованиях in vitro при инкубации с эпоэтином альфа было выявлено усиление инкорпорации 3Н-тимидина в эритроидных ядросодержащих клетках селезёнки (в культуре клеток селезёнки мыши). Исследования на культуре клеток костного мозга человека показали, что эпоэтин альфа специфически стимулирует эритропоэз и не оказывает влияния на лейкопоэз. Цитотоксического воздействия эпоэтина альфа на летки костного мозга человека не выявлено.
Эритропоэтин является фактором роста, который в основном стимулирует образование эритроцитов. Рецепторы к эритропоэтину могут присутствовать на поверхности различных опухолевых клеток.
Введение эпоэтина альфа сопровождается повышением уровня гемоглобина, гематокрита, сывороточного железа, что способствует улучшению кровоснабжения тканей и работы сердца. Наиболее значимый эффект эпоэтина альфа отмечен при анемиях, обусловленных хронической почечной недостаточностью, а также развившихся у пациентов с рядом злокачественных новообразований и системных заболеваний.
Фармакокинетика
Внутривенное введение
Период полувыведения (T½) эпоэтина альфа после многократного внутривенного введения составляет около 4 ч у здоровых добровольцев и около 5 ч у пациентов с хронической почечной недостаточностью. У детей T½ эпоэтина альфа составляет около 6 ч.
Подкожное введение
При подкожном введении концентрация эпоэтина альфа в плазме крови определяется существенно ниже, чем при внутривенном введении, время достижения максимальной концентрации (Сmах) эпоэтина альфа в плазме крови составляет около 12–18 ч после введения. Сmах эпоэтина альфа при подкожном введении составляет лишь ½ часть концентрации при внутривенном введении.
Препарат не обладает способностью к кумуляции — концентрацияэпоэтина альфа в плазме крови через 24 ч после первой инъекции определяется такой же, как через 24 ч после последней инъекции. При подкожном введении T½ эпоэтина альфа определить сложно, он составляет около 24 ч. Биодоступность эпоэтина альфа при подкожном введении значительно ниже, чем при его внутривенном введении, и составляет около 20%
Показания
Анемия у взрослых и детей, обусловленная хронической почечной недостаточностью (ХПН), в том числе:
- анемия вследствие хронической почечной недостаточности (ХПН) у детей и. взрослых на гемодиализе, а также у взрослых на перитонеальном диализе;
- тяжёлая анемия почечного генеза, сопровождающаяся клиническими симптомами у взрослых с ХПН, которым ещё не проводили гемодиализ.
- лечение анемии и уменьшение потребности в проведении переливания крови у взрослых, получающих лечение химиотерапевтическими препаратами по поводу солидных новообразований, злокачественной лимфомы или множественной миеломы, а также у лиц с высоким риском осложнений гемотрансфузий, обусловленным общим тяжёлым состоянием (в связи с сердечно-сосудистыми заболеваниями, если анемия отмечалась и до начала химиотерапии).
- для повышения эффективности переливания аутологичной крови в рамках предепозитной программы сбора крови перед хирургическими операциями у пациентов с уровнем гематокрита, равным 33–39 %, для облегчения сбора аутологичной крови и уменьшения риска, связанного с использованием аллогенных гемотранссрузии, если ожидаемая потреоность в переливаемой крови превышает количество, которое можно получить методом аутологичного сбора без применения эпоэтина альфа. Лечение показано пациентам при умеренно выраженной анемии (при концентрации гемоглобина 10–13 г/дл или 6,2–8,1 ммоль/л), без дефицита железа, если предполагается значительная кровопотеря, а также при обширных хирургических вмешательствах, когда может потребоваться большой объём переливаемой крови (5 и более объёмов у мужчин, 4 или более объёмов у женщин).
- для уменьшения степени риска при аллогенном переливании крови у взрослых, не имеющих дефицита железа, перед элективной ортопедической операцией, при наличии высокого риска осложнений при проведении гемотрансфузии. Применение препарата ограничено — только у пациентов с умеренно выраженной анемией (например, при концентрации гемоглобина 10- 13 г/дл), в том случае, если они не включены в программу сбора аутологичной крови перед операцией с ожидаемой кровопотерей от 900 до 1800 мл.
- анемия у ВИЧ-инфицированных пациентов, получающих терапию зидовудином, при уровне эндогенного эритропоэтина менее 500 МЕ/мл.
Противопоказания
- Повышенная чувствительность к действующему веществу или к любому компоненту, входящему в состав препарата.
- парциальная красноклеточная аплазия (ПККА), возникшая после лечения эритропоэтином;
- неконтролируемая артериальная гипертензия;
- хирургические пациенты, которые по каким-либо причинам не могут получать эффективное лечение для профилактики тромбозов;
- инфаркт миокарда или инсульт, произошедшие в течение 1 месяца до планируемого лечения; нестабильная стенокардия; пациенты с высоким риском тромбоза глубоких вен и тромбоэмболической болезни в анамнезе (в рамках повышения эффективности переливания аутологичной крови);
- тяжёлое поражение коронарных, периферических, сонных артерий, а также сосудов головного мозга, в том числе у пациентов, недавно перенёсших инфаркт миокарда или инсульт (в рамках предепозитной программы сбора крови перед обширной хирургической операцией и не участвующих в программе переливания аутологичной крови);
- все противопоказания, связанные с программой резервирования аутокрови, касаются пациентов, которые находятся на лечении эпоэтином альфа.
С осторожностью
Применение при беременности и в период грудного вскармливания
Надлежащие контролируемые исследования применения эпоэтина альфа у женщин во время беременности не проводились. По результатам исследований на животных выявлена репродуктивная токсичность. Вследствие этого, пациенткам с хронической почечной недостаточностью следует применять Бинокрит во время беременности, только если предполагаемая польза для матери значительно превышает риск для плода. Применение эпоэтина альфа не рекомендовано в период беременности или лактации пациентам, участвующим в программе сбора аутологичной крови перед хирургической операцией.
Способ применения и дозы
Лечение препаратом Бинокрит® должно проводиться под контролем врача-специалиста, имеющего соответствующую квалификацию и опыт лечения пациентов, которым показана терапия препаратами-стимуляторами эритропоэза.
Лечение симптоматической анемии у взрослых и детей с хронической почечной недостаточностью:
Бинокрит® у пациентов ХПН вводят внутривенно. В связи с тем, что клинические проявления анемии и остаточные явления могут различаться в зависимости от возраста, пола и общей тяжести заболевания, проводят индивидуальную оценку состояния каждого пациента.
Целевой уровень концентрации гемоглобина составляет 10–12 г/дл (6,2–7,5 ммоль/л) у взрослых и 9,5–11 г/дл (5,9–6,8 ммоль/л) у детей.
Не рекомендуется длительное повышение концентрации гемоглобина более 12 г/дл (7,5 ммоль/л). Если концентрация гемоглобина повышается более чем на 2 г/дл (1,25 ммоль/л) в месяц или если на протяжении длительного времени превышает 12 г/дл (7,5 ммоль/л), необходимо уменьшить дозу препарата Бинокрит® на 25 %. Если концентрация гемоглобина превышает 13 г/дл (8,1 ммоль/л), необходимо прекратить лечение до снижения уровня гемоглобина до 12 г/дл (7,5 ммоль/л), и затем возобновить терапию препаратом Бинокрит®, уменьшив начальную дозу на 25 %.
Вследствие межиндивидуальной вариабельности концентрация гемоглобина может оказаться выше или ниже оптимального (целевого) значения.
Лечение следует назначать таким образом, чтобы минимально эффективная доза препарата Бинокрит® обеспечивала необходимый контроль гемоглобина и клинических проявлений заболевания.
До начала лечения и в период лечения следует контролировать концентрацию железа в плазме крови, при необходимости назначают дополнительно препараты железа.
Взрослые пациенты, получающие гемодиализ:
Лечение проводится в два этапа:
Этап коррекции:
Внутривенно вводят Бинокрит® в дозе 50 МЕ/кг 3 раза в неделю. При необходимости дозу корректируют постепенно, в течение 4 недель. Увеличение или уменьшение дозы — не более 25 МЕ/кг 3 раза в неделю.
Этап поддерживающей терапии:
Коррекция дозы с целью поддержания необходимого уровня гемоглобина:
Нb 10–12 г/дл (6,2–7,5 ммоль/л).
Рекомендуемая суммарная еженедельная доза препарата Бинокрит® — от 75 до 300 МЕ/кг, внутривенно по 25–100 МЕ/кг 3 раза в неделю.
У пациентов с тяжёлой анемией (Нb <6 г/дл, или <3,75 ммоль/л), может понадобиться применение более высоких поддерживающих доз, чем у пациентов с более высокой концентрацией гемоглобина (<8 г/дл, или <5 ммоль/л).
Применение у детей, получающих гемодиализ
Этап коррекции:
Внутривенно вводят Бинокрит® в дозе 50 МЕ/кг 3 раза в неделю. При необходимости дозу корректируют постепенно, в течение 4 недель. Увеличение или уменьшение дозы — не более 25 МЕ/кг 3 раза в неделю.
Этап поддерживающей терапии:
Коррекция дозы с целью поддержания необходимого уровня гемоглобина:
Нb 9,5–11 г/дл (5,9–6,8 ммоль/л).
В большинстве случаев у детей с массой тела менее 30 кг необходимо применять более высокие поддерживающие дозы, чем у детей с более высокой массой тела и у взрослых. По имеющимся клиническим данным в течение 6 месяцев лечения целесообразно применение следующих доз препаратата в зависимости от массы тела пациентов:
| Доза (ЕД/кг, вводимые 3х/неделю) | ||
| Масса (кг) | Медиана | Обычная поддерживающая доза |
| < 10 | 100 | 75–150 |
| 10–30 | 75 | 60–150 |
| >30 | 33 | 30–100 |
У детей с тяжёлой анемией (Нb <6,8 г/дл, или < 4,25 ммоль/л) рекомендуется применение более высоких поддерживающих доз, чем у детей с более высокой концентрацией гемоглобина (Нb >6,8 г/дл, или >4,25 ммоль/л).
Взрослые пациенты, получающие перитонеальный диализ:
Течение проводится в два этапа:
Этап коррекции: начальная доза 50 МЕ/кг 2 раза в неделю внутривенно.
Этап поддерживающей терапии: коррекция дозы с целью поддержания необходимого уровня гемоглобина: Нb 10–12 г/дл (6,2–7,5 ммоль/л). Поддерживающая доза составляет от 25 до 50 МЕ/кг 2 раза в неделю, 2 равных инъекции.
Взрослые с почечной недостаточностью, которым не проводился диализ:
Лечение проводится в два этапа:
Этап коррекции: начальная доза составляет 50 МЕ/кг 3 раза в неделю внутривенно с последующим увеличением при необходимости на 25 МЕ/кг (3 раза в неделю) до достижения целевой дозы (увеличивать дозу следует постепенно как минимум в течение 4 недель).
Этап поддерживающей терапии: коррекция дозы с целью поддержания необходимого уровня гемоглобина: Нb 10–12 г/дл (6,2–7,5 ммоль/л). Поддерживающая доза составляет от 17 до 33 МЕ/кг 3 раза в неделю внутривенно.
Максимальная доза не должна превышать 200 МЕ/кг 3 раза в неделю.
Лечение анемии у пациентов после химиотерапии:
Препарат Бинокрит® вводят подкожно (при концентрации Нb <10 г/дл (6,2 ммоль/л). Доза препарата подбирается врачом с учётом тяжести анемии, возраста, пола и общей тяжести состояния пациента в индивидуальном порядке. Необходимо также учитывать колебания концентрации гемоглобина, корректируя применяемую дозу препарата с учётом нормальных значений концентрации гемоглобина 10 г/дл (6,2 ммоль/л) — 12 г/дл (7,5 ммоль/л). Не рекомендуется превышение концентрации гемоглобина более 12 г/дл (7,5 ммоль/л); рекомендации по корректировке дозы в подобных случаях приведены ниже.
Лечение необходимо назначать таким образом, чтобы минимально эффективная доза эпотина альфа обеспечивала необходимый контроль симптомов анемии. Терапию препаратом Бинокрит® следует продолжать в течение 1 месяца после завершения курса химиотерапии.
Начальная доза препарата составляет 150 МЕ/кг, вводится подкожно 3 раза в неделю. Возможно альтернативное применив препарата в дозе 450 МЕ/кг подкожно 1 раз в неделю.
В случае повышения концентрации гемоглобина минимум на 1 г/дл (>0,62 ммоль/л) или увеличения числа ретикулоцитов >40000 клеток/мкл относительно первоначальных показателей через 4 недели лечения, доза препарата составляет 150 МЕ/кг 3 раза в неделю или 450 МЕ/кг 1 раз в неделю, и остаётся без изменений.
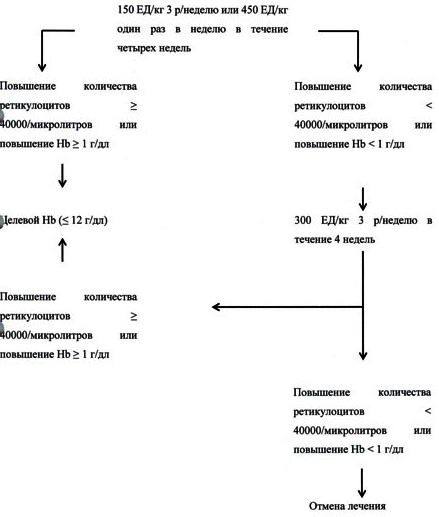
При повышении концентрации гемоглобина <1 г/дл (<0,62 ммоль/л) и увеличении числа ретикулоцитов <40000 клеток/мкл относительно первоначальных показателей, необходимо увеличить дозу препарата до 300 МЕ/кг 3 раза в неделю. Если по истечении ещё 4 недель лечения при дозе 300 МЕ/кг 3 раза в неделю концентрация гемоглобина повысится >1 г/дл (>0,62 ммоль/л) или число ретикулоцитов увеличится >40000 клеток/мкл, доза препарата должна оставаться прежней и составлять 300 МЕ/кг 3 раза в неделю. Однако если увеличение концентрации гемоглобина < 1 г/дл (<0,62 ммоль/л) и прирост числа ретикулоцитов <40000 клеток/мкл относительно первоначальных показателей, терапия препаратом Бинокрит® считается малоэффективной, её следует прекратить.
Рекомендованный режим назначения описан в следующей схеме:
Корректировка дозы для поддержания концентрации гемоглобина в пределах 10–12 г/дл:
Если концентрация гемоглобина повышается более чем на 2 г/дл (1,25 ммоль/л) в месяц или если уровень гемоглобина превышает 12 г/дл (7,5 ммоль/л), необходимо сократить дозу препарата на 25–50 %. Если концентрация гемоглобина превышает 13 г/дл (8,1 ммоль/л), необходимо прекратить лечение до снижения его значения до 12 г/дл (7,5 ммоль/л), а затем возобновить терапию эпоэтином альфа, уменьшив начальную дозу на 25 %.
Взрослые пациенты, участвующие в программе сбора аутологичной крови перед хирургическими операциями:
Бинокрит® вводят внутривенно, предварительно завершив процедуру сдачи крови. Лациентам с анемией лёгкой степени (при уровне гематокрита 33–39 %), которым требуется > 4 единиц крови, необходимо проводить лечение препаратом Бинокрит® в дозе 600 МЕ/кг массы тела 2 раза в неделю на протяжении 3 недель до хирургического вмешательства.
Всем пациентам, получающим Бинокрит®, следует дополнительно назначать препараты железа (внутрь в дозе 200 мг/сут.) в течение всего курса терапии. Применение препарата железа следует назначать до начала терапии препаратом Бинокрит®, как можно раньше, за несколько недель до начала сбора аутологичной крови.
Взрослые пациенты, подлежащие элективной ортопедической хирургии:
Бинокрит® вводят подкожно.
Рекомендуемая доза препарата Бинокрит® — 600 МЕ/кг 1 раз в неделю в течение 3-х недель, предшествующих операции (за 21, 14 и 7 дней до операции), а также в день операции. Если предоперационный период короче 3-х недель, Бинокрит® следует назначать ежедневно в дозе 300 МЕ/кг 10 дней подряд, перед хирургическим вмешательством, в день операции и в течение 4-х дней после неё. Если в предоперационный период концентрация гемоглобина составляет 15 г/дл (9,38 ммоль/л) или выше, применение препарата необходимо прекратить. Следует убедиться, что до начала лечения препаратом Бинокрит® у пациентов нет дефицита железа.
Все пациенты, получающие терапию препаратом Бинокрит®, должны получать необходимое количество двухвалентного железа (внутрь 200 мг/сут.) в течение всего курса терапии.
Профилактика и лечение анемии у пациентов с ВИЧ-инфекцией:
Внутривенное введение препарата Бинокрит® в дозе 100–150 МЕ/кг 3 раза в неделю является эффективным у ВИЧ-пациентов, получающих терапию Зидовудином, при условии, что уровень сывороточного эндогенного эритропоэтина менее 500 МЕ/мл, а доза Зидовудина составляет менее 4200 мг/неделю. При подкожном введении доза Бинокрита может быть уменьшена в 1,5 раза.
Способ введения
Бинокрит® — стерильный, не содержащий консервантов препарат, предназначенный исключительно для одноразового применения. Следует вводить необходимое количество препарата.
Препарат не следует вводить в виде внутривенной инфузии или смешивать его с другими лекарственными средствами.
- Внутривенная инъекция: продолжительность инъекции составляет 1–5 минут в зависимости от общего объёма дозы. При гемодиализе может применяться болюсная инъекция во время процедуры диализа через удобный венозный порт в диализной линии. Альтернативой может быть инъекция, сделанная в конце процедуры диализа через фистульную иглу, затем вводят 10 мл изотонического раствора натрия хлорида для прочистки иглы и обеспечения удовлетворительного введения препарата в кровоток.
Пациентам, с возможными температурными реакциями на внутривенное введение препаратов, рекомендуется медленное введение препарата.
- Подкожная инъекция: не следует превышать максимальный объём инъекции (1 мл) на одно место введения. В случае введения больших объёмов необходимо выбирать большее количество мест для инъекций. Препарат вводят в мышцу бедра или в область передней брюшной стенки.
Побочное действие
По данным Всемирной организации здравоохранения (ВОЗ) нежелательные эффекты классифицированы в соответствии с частотой их развития следующим образом: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1,000 до <1/100), редко (от ≥1/10,000 до <1/1,000), очень редко (<1/10,000); частота неизвестна — по имеющимся данным установить частоту возникновения не представлялось возможным.
Кровь и лимфатическая система:
нечасто: тромбоцитемия (у пациентов со злокачественными новообразованиями);
частота неизвестна: парциальная красноклеточная аплазия (ПККА), опосредованная через антитела1, тромбоцитемия (у пациентов с ХПН).
Иммунная система
частота неизвестна: анафилактическая реакция, повышенная чувствительность.
Нервная система
очень часто: головная боль (у пациентов со злокачественными новообразованиями);
часто: судороги (у пациентов ХПН), головная боль (у пациентов ХПН);
нечасто: геморрагический инсульт2, судороги (у пациентов со злокачественными новообразованиями);
частота неизвестна: цереброваскулярные нарушения, гипертоническая энцефалопатия, транзиторные ишемические атаки.
частота неизвестна: тромбоз сетчатки.
Сердечно-сосудистая система
часто: тромбоз глубоких вен (у пациентов со злокачественными новообразованиями), повышение артериального давления2;
частота неизвестна: тромбоз глубоких вен (у пациентов с ХПН), артериальный тромбоз, гипертонический криз, инфаркт миокарда.
Органы дыхания
часто: тромбоэмболия лёгочной артерии (у пациентов со злокачественными новообразованиями);
частота неизвестна: тромбоэмболия лёгочной артерии (у пациентов с ХПН) 2.
Желудочно-кишечный тракт
очень часто: тошнота;
часто: диарея (у пациентов со злокачественными новообразованиями), рвота;
нечасто: диарея (у пациентов с ХПН).
Кожа и её придатки
часто: кожная сыпь;
частота неизвестна: ангионевротический отёк, крапивница.
Костно-мышечная система
очень часто: артралгия (при ХПН);
часто: артралгия (у пациентов со злокачественными новообразованиями);
нечасто: миалгия (у пациентов со злокачественными новообразованиями);
частота неизвестна: миалгия (при ХПН).
Врождённые, семейные/генетические нарушения
частота неизвестна: порфирия.
Организм в целом
очень часто: гипертермия (у пациентов со злокачественными новообразованиями); гриппоподобное состояние (при ХПН);
часто: гриппоподобное состояние (у пациентов со злокачественными новообразованиями);
частота неизвестна: неэффективность препарата, периферические отёки, гипертермия (при ХПН), реакции в месте введения.
Лабораторные показатели
частота неизвестна: антитела к эритропоэтину1.
Другие
часто: тромбоз шунта диализного оборудования (у пациентов с ХПН).
1 Частота проявлений не может быть оценена на основании клинических исследований.
2 Включая случаи со смертельным исходом
Резюме профиля безопасности: У пациентов, страдающих онкологическими заболеваниями и у пациентов с хронической почечной недостаточностью, в период лечения эпоэтином альфа наиболее часто наблюдается такая нежелательная реакция как дозозависимое повышение артериального давления и усиление существующей гипертензии. У таких пациентов, особенно в начале лечения, необходимо регулярно контролировать показатели артериального давления. Другими нежелательными реакциями, часто наблюдающимися при применении эпоэтина альфа, являются следующие: тромбоз глубоких вен, эмболия лёгочной артерии, обмороки, диарея, тошнота, головная боль, гриппоподобные симптомы, повышенная температура, сыпь и рвота. Гриппоподобные симптомы включают в себя головную боль, артралгию, миалгию и повышенную температуру. Как правило, они наблюдаются в начале лечения. Частота симптоматики варьирует в зависимости от показаний.
Передозировка
Терапевтический диапазон препарата широк. При передозировке возможно возникновение симптомов, которые отражают крайнюю степень проявления фармакологического действия гормона (повышение концентрации гемоглобина или гематокрита). При исключительно высоких уровнях гемоглобина или гематокрита возможно применение флеботомии. В случае необходимости назначается симптоматическая терапия.
Взаимодействие с другими лекарственными средствами
Данных о взаимодействии эпоэтина альфа с другими лекарственными средствами нет. Однако, при одновременном применении с циклоспорином возможно взаимодействие, поскольку препарат связывается с эритроцитами. Если лечение препаратом Бинокрит® проводится одновременно с циклоспорином, необходимо контролировать концентрацию циклоспорина в зависимости от степени повышения гематокрита.
Нет данных о взаимодействии между эпоэтином альфа и гранулоцитарным колониестимулирующим фактором (Г-КСФ) или гранулоцитарно-моноцитарным холониестимулирующим фактором (ГМ-КСФ).
Во избежание несовместимости или снижения активности, не рекомендуется смешивать с растворами и другими лекарственными препаратами.
Особые указания
Общая информация
При назначении препарата Бинокрит® у всех пациентов необходимо проверять и строго контролировать артериальное давление. Следует с осторожностью применять эпоэтин альфа у пациентов с артериальной гипертензией, если они не получают необходимого лечения, назначенное лечение неадекватно или гипертензия плохо поддаётся контролю. В этом случае может возникнуть необходимость начать или усилить антигипертензивную терапию, которая уже применялась. Если нормализовать артериальное давление не удаётся, лечение эпоэтином альфа следует прекратить. Бинокрит® с осторожностью применяют при наличии эпилепсии и хронической печёночной недостаточности.
Пациенты с хронической почечной недостаточностью и онкологические пациенты должны регулярно контролировать уровень гемоглобина до достижения стабильных показателей и периодически после этого.
Тщательный контроль уровня гемоглобина обязателен для всех пациентов в связи с потенциально повышенным риском тромбоэмболических осложнений и увеличением количества фатальных случаев, когда пациенты получали лечение при уровне гемоглобина, превышающем установленную норму для применения препарата по показаниям.
Вo время лечения препаратом Бинокрит® может наблюдаться умеренное дозозависимое увеличение количества тромбоцитов (в пределах нормы). При продолжении курса терапии данный показатель вновь снижается. В течение первых 8 недель после начала терапии рекомендуется регулярно контролировать количество тромбоцитов.
До начала терапии необходимо исключить все иные причины возникновения анемии (дефицит железа, гемолиз, кровопотеря, дефицит витамина B12) или фолиевой кислоты). В большинстве случаев уровень ферритина в сыворотке крови снижается при одновременном увеличении гематокрита.
Чтобы гарантировать оптимальный ответ на эпоэтин альфа, требуются адекватные запасы железа:
- приём железа, например, 200–300 мг Fe2+ /сутки внутрь (100–200 мг Fe2+ /сутки для пациентов детей), рекомендуется пациентам хронической почечной недостаточностью с уровнями ферритина ниже 100 нанограмм/мл;
- приём железа внутрь 200–300 мг Fe2+ /сутки рекомендуется всем онкологическим пациентам с насыщением трансферрина ниже 20 %.
Все эти дополнительные факторы анемии необходимо обязательно учитывать при принятии решения о повышении дозы эпоэтина альфа у пациентов раком.
Очень редко наблюдалось развитие или обострение порфирии у пациентов, получавших терапию эпоэтином альфа. Эпоэтин альфа следует использовать с осторожностью у пациентов порфирией.
Все перечисленные дополнительные факторы анемии также следует учитывать при увеличении дозы препарата Бинокрит® у пациентов с новообразованиями. В периооперационный период необходимо тщательно следить за всеми показателями крови.
Чтобы улучшить отслеживаемость нежелательных явлений при применении препаратов, стимулирующих эритропоэз, следует точно записывать (или указывать) торговое название назначенного стимулирующего эритропоэз препарата в карте пациента. Смену терапии одним препаратом, стимулирующим эритропоэз, на другой следует проводить только под соответствующим наблюдением.
Парциальная красноклеточная аплазия (ПККА)
После нескольких месяцев или лет лечения препаратом Бинокрит® с применением подкожных инъекций случаи развития парциальной красноклеточной аплазии (ПККА), опосредованной через антитела, наблюдались очень редко. Если у пациентов резко снижается эффективность терапии вследствие уменьшения концентрации гемоглобина (1–2 г/дл в месяц) на фоне возросшей потребности в гемотрансфузиях, необходимо проверить количество ретикулоцитов и изучить типичные причины отсутствия реакции на препарат (например, дефицит железа, фолиевой кислоты или витамина B12, интоксикация алюминием, инфекции или воспаление, кровотечение или гемолиз). Есть данные о таких проявлениях у пациентов гепатитом C, получавших лечение интерфероном и рибавирином одновременно с эпоэтином альфа. Бинокрит® не предназначен для лечения анемии, обусловленной гепатитом C.
Если содержание ретикулоцитов с учётом анемии (например, ретикулоцитарный индекс) низкое (<20000/мм3 или <20000/мкл или <0,5 %), количество тромбоцитов и лейкоцитов в норме и никакой иной причины снижения эффективности не выявлено, необходимо определить наличие антител к эритропоэтину и провести обследование костного мозга с целью диагностирования парциальной красноклеточной аплазии (ПККА).
При подозрении на появление ПККА, опосредованной через антитела к эритропоэтину, следует немедленно прекратить терапию препаратом Бинокрит®. Запрещается назначать терапию любым другим препаратом эритропоэтина из-за риска перекрёстной реакции. При наличии показаний пациентам может назначаться необходимая терапия, например, гемотрансфузии.
Пациенты с хронической почечной недостаточностью
Данные по иммуногенности при подкожном введении препарата Бинокрит пациентам с риском развития ПККА, опосредованной через антитела, например пациентам с почечной анемией, ограничены. Вследствие этого, пациентам с почечной анемией препарат должен вводиться внутривенно.
С целью минимизации рисков усиления гипертензии для пациентов с хронической почечной недостаточностью скорость повышения уровня гемоглобина должна составлять примерно 1 г/дл (0,62 ммоль/л) в месяц и не должна превышать 2 г/дл (1,25 ммоль/л) в месяц.
У пациентов с хронической почечной недостаточностью концентрация гемоглобина на поддерживающей стадии лечения не должна превышать 12 г/дл (подробнее см. раздел «Способ применения и дозы»). Результаты клинических исследований показали увеличение риска фатальных исходов и тяжёлых сердечно-сосудистых расстройств при введении эритропоэз-стимулирующих препаратов с целью увеличения концентрации гемоглобина более 12 г/дл (7,5 ммоль/л).
При проведении клинических исследований в контролируемых условиях не выявлено значительных преимуществ, связанных с применением эпоэтинов на фоне увеличения концентрации гемоглобина выше уровня, необходимого для контролирования симптомов анемии и предупреждения гемотрансфузий. У пациентов на гемодиализе отмечались случаи тромбозов шунта, в частности, при склонности к гипотонии или вследствие формирования артериовенозных фистул (например, стеноза, аневризмы и т. д.). Таким пациентам рекомендуется ранняя коррекция шунта и профилактика тромбоза, например, с помощью ацетилсалициловой кислоты.
В отдельных случаях наблюдалась гиперкалиемия. Лечение анемии может приводить к повышению аппетита и увеличению потребности в калии и белке. Периодически следует корректировать схему проведения диализа с целью поддержания необходимых показателей мочевины, креатинина и калия. У пациентов с хронической почечной недостаточностью необходимо проверять содержание электролитов в сыворотке крови. При обнаружении повышенного (или повышающегося) уровня сывороточного калия следует оценить целесообразность отмены лечения эпоэтином альфа до нормализации уровня калия. Во время лечения эпоэтином альфа часто требуется повышение дозы гепарина при проведении гемодиализа вследствие увеличения гематокритного числа. Если гепаринизация не может быть максимально эффективной, может потребоваться отмена схемы процедур диализа.
Согласно имеющимся данным, лечение анемии эпоэтином альфа у взрослых пациентов с почечной недостаточностью, которым ещё не проводится диализ, не вызывает прогрессирования почечной недостаточности.
Взрослые онкологические пациенты с симптоматической анемией, проходящие курс химиотерапии
Эритропоэтины являются факторами роста, которые, преимущественно, стимулируют образование эритроцитов. Рецепторы эритропоэтина могут быть экспрессированы на поверхности различных опухолевых клеток. Как и при воздействии любых факторов роста, интерес представляет тот факт, что эпоэтины могут стимулировать рост опухоли. В контролируемых клинических исследованиях при использовании эпоэтина альфа и других стимулирующих эритропоэз препаратов показано, что:
- снизился местно-регионарный контроль у пациентов с распространённым раком головы и шеи, получающих лучевую терапию при назначении препарата Бинокрит® до достижения уровня гемоглобина выше 14 г/дл (8,7 ммоль/л)
- сократилась общая выживаемость и увеличилась частота смертности в связи с прогрессированием заболевания у пациентов метастатическим раком молочной железы, получающих химиотерапию при назначении эпоэтина альфа до достижения уровня гемоглобина 12–14 г/дл (7,5–8,7 ммоль/л)
- повысился риск смерти при назначении до достижения гемоглобина 12 г/дл (7,5 ммоль/л) у пациентов с активным злокачественным заболеванием, не получающих химиотерапию/лучевую терапию. Стимулирующие эритропоэз препараты не показаны для использования в данной группе пациентов.
Принимая во внимание вышесказанное, в некоторых клинических ситуациях переливания крови могут быть предпочтительным средством при лечении анемии у пациентов с онкологическими заболеваниями.
Решение о назначении рекомбинантных эритропоэтинов необходимо принимать, учитывая соотношение пользы и возможных рисков для каждого пациента индивидуально, и особенности клинической ситуации. Следует учитывать следующие факторы: тип и стадия развития новообразования, степень анемии, ожидаемую продолжительность жизни, обстановку, в которой пациент будет проходить лечение, пожелания самого пациента.
При оценке целесообразности терапии эпоэтином альфа (риск переливания крови для пациента) у онкологических пациентов, получающих химиотерапию, необходимо учитывать задержку в 2–3 недели после введения эпоэтина альфа до образования эритроцитов.
С целью минимизации риска развития тромботических явлений необходимо контролировать, чтобы уровень гемоглобина и скорость его увеличения не превышали допустимых показателей.
Вследствие увеличения количества случаев венозных тромботических осложнений у онкологических пациентов, получающих эритропоэз-стимулирующие препараты, следует тщательно оценивать такой риск и пользу от лечения (эпоэтином альфа), особенно у онкологических пациентов с повышенным риском развития венозных тромботических осложнений, например, на фоне ожирения или наличия венозных тромботических заболеваний в семейном анамнезе (в том числе глубокого венозного тромбоза или тромбоэмболии лёгочной артерии). Организовано клиническое испытание с исследуемым препаратом (исследование BEST) у женщин с метастатическим раком молочной железы, чтобы определить, улучшает ли исходы лечения терапия эпоэтином альфа, выходящая за рамки коррекции анемии. В этом исследовании частота летальных тромбоэмболических явлений оказалась выше у пациентов, получающих эпоэтин альфа, чем у пациентов, получающих плацебо.
Взрослые пациенты, участвующие в программе сбора аутологичной крови перед хирургическими операциями:
Необходимо соблюдать все особые меры предосторожности, относящиеся к проведению программ по сбору аутологичной крови, особенно при регулярных переливаниях крови.
Пациенты, подлежащие элективной ортопедической хирургии
Необходимо установить причину анемии и, по возможности, назначить лечение перед началом терапии эпоэтином альфа. У таких пациентов может возникать риск развития тромботических явлений, который необходимо тщательно оценивать при назначении лечения пациентам данной группы.
Пациенты, подлежащие элективной ортопедической хирургии, должны получать адекватную антитромботическую профилактику в связи с наличием риска развития венозных тромботических осложнений у хирургических пациентов, в особенности у страдающих сердечно-сосудистыми заболеваниями. Кроме того, необходимо соблюдать особые меры предосторожности для пациентов с предрасположенностью к развитию тромбоза глубоких вен конечностей. У пациентов с первоначальным уровнем гемоглобина >13 г/дл (>8,1 ммоль/л) повышен риск послеоперационных громботических/венозных осложнений. Вследствие этого препарат не следует назначать пациентам с первоначальным уровнем гемоглобина >13 г/дл (>8,1 ммоль/л).
Вспомогательные вещества
Данный лекарственный препарат содержит менее 1 ммоль натрия (23 мг) в одном предварительно заполненном шприце, то есть фактически не содержит натрия.
Влияние на способность управлять транспортными средствами, механизмами
Бинокрит® не влияет на способность управлять автотранспортными средствами или работать с механизмами.
Форма выпуска
Раствор для внутривенного и подкожного введения 16,8 мкг/мл (1000 МЕ/0,5 мл, 2000 МЕ/мл), 84 мкг/мл (3000 МЕ/0,3 мл, 4000 МЕ/0,4 мл, 5000 МЕ/0,5 мл, 6000 МЕ/0,6 мл, 8000 МЕ/0,8 мл, 10000 МЕ/мл), 336 мкг/мл (20000 МЕ/0,5 мл, 30000 МЕ/0,75 мл, 40000 МЕ/мл).
По 0,5 мл (1000 МЕ) или 1 мл (2000 МЕ) раствора для внутривенного и подкожного введения 16,8 мкг/мл, 0,3 мл (3000 МЕ), 0,4 мл (4000 МЕ), 0,5 мл (5000 МЕ), 0,6 мл (6000 МЕ), 0,8 мл (8000 МЕ) или 1 мл (10000 МЕ) раствора для внутривенного и подкожного введения 84 мкг/мл, 0,5 мл (20000 МЕ), 0,75 мл (30000 МЕ) или 1 мл (40000 МЕ) раствора для внутривенного и подкожного введения 336 мкг/мл в однодозовых градуированных (с ценой деления 0,1 мл) шприцах из прозрачного бесцветного боросиликатного стекла типа I (Евр. Ф.), снабжённых шток-поршнем из полипропилена с бромбутилкаучуковым уплотнителем, покрытым фторполимером, и инъекционной иглой из нержавеющей стали 27 G × 1/2 с резиновым безлатексным защитным колпачком и внешним колпачком из полипропилена (для предотвращения затупления иглы), а также специальным колпачком безопасности для иглы после проведённой инъекции (для предупреждения травматизации вследствие укола иглой по неосторожности) или без такового.
По 1 или 3 шприца помещают в контурную упаковку из прозрачного бесцветного листового пластика (коррекс) и запечатывают прозрачной плёнкой. По 1 коррексу с 1 шприцем или по 2 коррекса с 3 шприцами вместе с инструкцией по применению помещают в картонную пачку.
Хранение
При температуре от 2 до 8 °C.
Не замораживать.
Хранить в недоступном для детей месте.
Специальные меры предосторожности при уничтожении неиспользованного препарата
Нет необходимости в специальных мерах предосторожности при уничтожении неиспользованного препарата.
Срок годности
2 года.
Не использовать по истечении срока годности, указанного на упаковке.
Примечание:
Возможно однократное хранение препарата при комнатной температуре (не выше 25 °C) в течение 72 часов. По истечении 72 часов препарат использовать не рекомендуется, и он должен быть утилизирован.
Условия отпуска из аптек
Отпускают по рецепту
Производитель
IDT Biologika, GmbH, Германия
Подробнее по теме
Ознакомьтесь с дополнительными сведениями о препарате Бинокрит:
