Артлегиа
Лекарственная форма
раствор для подкожного введения
Состав
Состав на 1 мл:
Действующее вещество: олокизумаб — 160,0 мг
Вспомогательные вещества: натрия хлорид, полисорбат 80, L-гистидина гидрохлорида моногидрат, сорбитол, вода для инъекций.
Описание
Прозрачная или слегка опалесцирующая жидкость от бесцветного до светло-жёлтого цвета.
Фармакологические свойства
Олокизумаб представляет собой гуманизированное (с присоединённым гипервариабельным участком) моноклональное антитело, относящееся к изотипу иммуноглобулина (immunoglobulin, Ig) G4/каппа. Олокизумаб селективно связывается с человеческим ИЛ-6 и эффективно нейтрализует эффекты ИЛ-6 in vivo и in vitro. Полученные данные свидетельствуют о том. что олокизумаб не связывается в значительной степени с другими молекулами семейства ИЛ-6 и не влияет на их функционирование, а также не активирует сигнальный путь ИЛ-6.
Фармакодинамика
В двойных слепых рандомизированных клинических исследованиях 2 фазы подкожное введение олокизумаба в дозе от 60 до 480 мг/мес пациентам со среднетяжёлым или тяжёлым ревматоидным артритом вызывало выраженное снижение уровня С-реактивного белка (СРБ) в плазме в течение 7 дней от начала лечения, сохранявшееся в течение не менее 10 недель после однократного введения, и в течение всего периода терапии при многократном введении препарата.
У пациентов со среднетяжёлым или тяжёлым ревматоидным артритом, недостаточно контролируемым терапией метотрексатом, подкожное введение олокизумаба в дозе 64 мг каждые 2 недели (к2н) или 64 мг каждые 4 недели (к4н) вызывало резкое снижение среднего уровня СРБ в плазме ко 2 неделе лечения. Низкие уровни СРБ сохранялись в течение 24 недель на протяжении всего периода лечения.
Клиническая эффективность
Эффективность подкожного введения олокизумаба в дозе 64 мг каждые 2 недели (к2н) и каждые 4 недели (к4н) была изучена у пациентов со среднетяжелым или тяжёлым ревматоидным артритом, недостаточно контролируемым терапией метотрексатом, в клиническом исследовании CREDO1.
Олокизумаб в обеих дозировках был значительно эффективнее плацебо в отношении снижения активности ревматоидного артрита вне зависимости от пола, индекса массы тела, активности заболевания, уровня антител к ревматоидному фактору и/или циклическому цитрирулированному пептиду. Длительность периода от постановки диагноза до начала лечения и продолжительность предшествующей терапии метотрексатом также не влияла на клиническую эффективность препарата. Кроме того, доля пациентов, достигших низкой активности заболевания и ремиссии, была значимо выше среди получавших олокизумаб по сравнению с плацебо. У пациентов, получавших олокизумаб, также чаще отмечалось улучшение качества жизни, уменьшение боли и количества болезненных и припухших суставов. Воздействие олокизумаба было заметным уже через 4 недели лечения, выраженный эффект развивался приблизительно через 12 недель от начала введения препарата и сохранялся в течение не менее чем 24 недель.
Фармакокинетика
Абсорбция
Биодоступность олокизумаба оценивалась на основании данных, полученных для 173 пациентов с лёгким или умеренным ревматоидным артритом, получавших олокизумаб в различных дозах в течение 12 недель, объединённых с данными, полученными у 40 пациентов с лёгким или умеренным ревматоидным артритом после однократного введения различных доз олокизумаба и данными, полученными у 41 здорового добровольца после однократного введения различных доз олокизумаба. При подкожном введении биодоступность составляет 63 % (доля относительной стандартной ошибки (% ОСО) = 4,9 %).
После однократного подкожного введения олокизумаба пациентам с лёгким или умеренным ревматоидным артритом в дозах от 0,3 до 6 мг/кг максимальная концентрация препарата в крови (Cmax) дозозависимо возрастала. Время достижения Cmax составляло от 4 до 12 дней, при этом поддающиеся определению уровни олокизумаба сохранялись приблизительно до 16 недель.
После однократного подкожного введения олокизумаба в дозе 64 мг пациентам с ревматоидным артритом средней и тяжёлой степени, недостаточно контролируемым на фоне лечения метотрексатом, Cmax достигалась в среднем через 7–10 дней (Таблица 1).
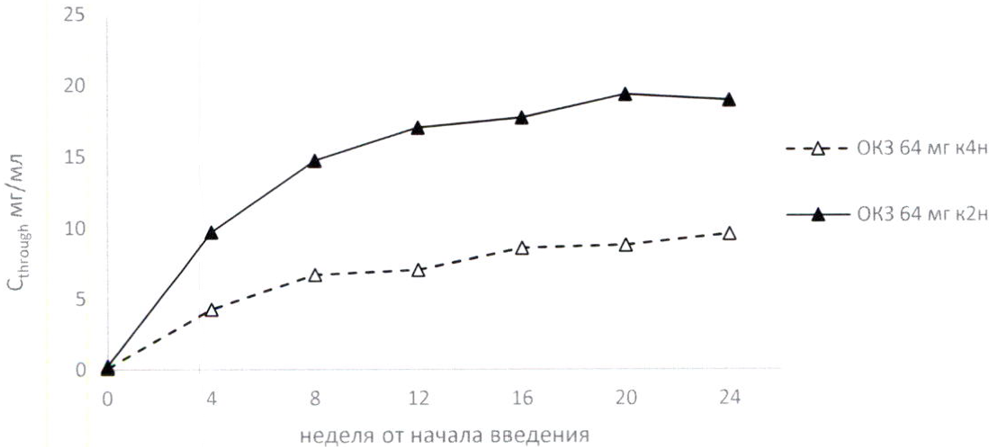
При многократном введении стационарная концентрация олокизумаба в крови нарастала в течение начального периода терапии и достигала равновесного состояния через 16 (64 мг к4н) и 14 (64 мг к2н) недель от начала лечения (Таблица 1. Рисунок 1).
| ФК параметр | Исходные значения | Неделя 20 | ||
| ОКЗ 64 мг к4п N = 18 | ОКЗ 64 мг к2н N = 18 | ОКЗ 64 мг к4н N = 18 | ОКЗ 64 мг к2н N = 18 | |
| Cmax (мкг/мл) %CV | 6,18 50,0 | 6,22 39,2 | 17,00 55,7 | 21,55 25,0 |
| AUC0–t* (мкг × ч/мл) %CV | 2886 45,3 | 1556 38,9 | 8411 29,9 | 5485 31,8 |
| tmax (ч) Медиана Мин. – макс. | 190,2 166,5 92,8 – 402,3 | 234,4 236,7 95,8 – 359,2 | 244,5 167,6 95,4 – 670,7 | 127,8 96,7 0,0 – 334,7 |
РА — ревматоидный артрит; ОКЗ — олокизумаб; к2н — каждые 2 недели; к4н — каждые 4 недели; Cmax — максимальная концентрация препарата в крови; AUC0–t — площадь под кривой концентрация-время; tmax — время достижения максимальной концентрации препарата; *AUC для введения к4н рассчитывалась за период 672 часа (28 дней) и для введения к2н за период 336 часов (14 дней)
Рисунок 1. Динамика нарастания стационарной концентрации (Cthrough) при многократном подкожном введении пациентам с ревматоидным артритом средней и тяжёлой степени
Биотрансформация
В исследовании in vitro на криоконсервированных гепатоцитах человека олокизумаб обращал ингибиторный эффект ИЛ-6 на активность CYP1 A1/2, 2B6, 2C9, ЗA4/5 и 2C19, а также на активность NTCP.
Элиминация
Оценки клиренса олокизумаба у пациентов с лёгким или умеренным ревматоидным артритом составляли 0,17 л/сут (доля относительной стандартной ошибки [% ОСО] = 4,9 %) с низкой или средней индивидуальной вариабельностью.
Фармакокинетическая-фармакодинамическая зависимость Уровень снижения СРВ у пациентов с активным ревматоидным артритом, получавших олокизумаб, не зависел от дозы препарата. Кроме того, у пациентов с лёгким и умеренным ревматоидным артритом была выявлена положительная корреляция концентрации олокизумаба в плазме с уровнем нейтропении, повышением уровней ACT, АЛТ и триглицеридов в плазме, хотя величина эффекта была невелика. Также к 14 дню после введения олокизумаба наблюдалось стойкое снижение уровня VEGF и амилоидного сывороточного белка А во всех терапевтических группах без зависимости от дозы.
Показания
Терапия пациентов старше 18 лет с ревматоидным артритом средней или высокой степени активности в комбинации с метотрексатом, при недостаточной эффективности монотерапии метотрексатом.
Противопоказания
- Гиперчувствительность к олокизумабу, любому компоненту препарата в анамнезе.
- Активные инфекционные заболевания (в том числе и туберкулёз).
- Детский возраст до 18 лет.
- Наследственная непереносимость фруктозы (препарат содержит сорбитол).
- Беременность.
- Период грудного вскармливания.
С осторожностью
- У пациентов с серьёзными или оппортунистическими инфекциями в анамнезе; с сопутствующими заболеваниями и состояниями, являющимися факторами риска развития инфекций (сахарный диабет, почечная недостаточность, приём иммуносупрессивных препаратов, пожилой возраст и др.).
- У пациентов, контактировавших с больными туберкулёзом. Перед применением препарата Артлегиа у таких пациентов следует оценить соотношение риска и пользы применения препарата.
- У пациентов с дивертикулитом или перфорациями кишечника в анамнезе и другими факторами риска перфорации кишечника.
- У пациентов с нарушениями функции печени и печёночной недостаточностью.
Беременность и лактация
Перед назначением препарата Артлегиа женщинам детородного возраста следует выполнить тест на беременность. Лечащий врач должен подробно разъяснить риски применения препарата Артлегиа во время беременности и проинструктировать пациентку, способную к деторождению, о необходимости использования высокоэффективных методов контрацепции и выполнения регулярных тестов на беременность во время лечения и в течение по крайней мере 6 месяцев после получения последней дозы препарата Артлегиа. В случае, если пациентка, получающая препарат Артлегиа, забеременеет, она должна немедленно прекратить применение препарата и обратиться к врачу.
Беременность
Применение препарата Артлегиа у беременных систематически не изучалось. В связи с тем, что препарат Артлегиа показан к применению в комбинации с метотрексатом, имеющим хорошо известное тератогенное действие, применение препарата Артлегиа при беременности не рекомендуется.
В исследованиях на животных обнаружена репродуктивная токсичность. Предполагается, что ИЛ-6 играет важную роль в раскрытии шейки матки и, возможно, в рождении плаценты.
Таким образом, применение препарата Артлегиа может нарушать родовую деятельность.
Лактация
Проникновение олокизумаба в грудное молоко не изучалось. Клинические данные о риске для ребёнка, находящегося на грудном вскармливании, отсутствуют. Так как препарат Артлегиа показан к применению в комбинации с метотрексатом, который секретируется в грудное молоко, рекомендуется прекратить грудное вскармливание при назначении препарата.
Фертильность
Клинические данные о влиянии олокизумаба на фертильность у человека отсутствуют.
В исследованиях на животных отрицательного воздействия олокизумаба на фертильность самцов и самок яванских макак не обнаружено.
Способ применения и дозы
Препарат Артлегиа вводится подкожно, в область бедра или передней брюшной стенки, 0,4 мл раствора с концентрацией 160 мг/мл единовременно. Перед введением раствор следует нагреть до комнатной температуры. Время хранения препарата при температуре >8 °C не должно превышать 4 часов.
Первое применение препарата проводят под контролем квалифицированного медицинского сотрудника. После первой инъекции следует наблюдать за состоянием пациента в течение 30 минут. После обучения технике выполнения подкожных инъекций под контролем медицинского сотрудника пациент (или лицо, осуществляющее за ним уход) может вводить препарат самостоятельно. Решение о возможности самостоятельного введения препарата Артлегиа пациентом принимает врач, имеющий опыт диагностики и лечения ревматоидного артрита.
Для введения препарата Артлегиа следует использовать только шприцы для однократного применения.
Пропуск дозы
Если была пропущена очередная инъекция препарата, следует ввести пропущенную дозу как можно быстрее, при этом интервал между любыми двумя введениями должен составлять не менее половины интервала выбранного режима дозирования (см. Таблица 2).
| Режим дозирования | Интервал от даты пропуска | Действие |
| ОКЗ 64 мг к4н | ≤14 дней | Выполнить инъекцию вместо пропущенной и далее по графику |
| >14 дней | Отменить пропущенную инъекцию | |
| ОКЗ 64 мг к2н | ≤7 дней | Выполнить инъекцию вместо пропущенной и далее по графику |
| >7 дней | Отменить пропущенную инъекцию |
ОКЗ — олокизумаб; к2н — каждые 2 недели; к4н — каждые 4 недели
Прекращение применения препарата
Терапию препаратом Артлегиа следует отменить, если у пациента наблюдается:
Повышение биохимических показателей функции печени, соответствующее следующим условиям:
- повышение уровня ACT или АЛТ >8 верхних границ нормы (ВГН) в любое время независимо от уровня общего билирубина или сопутствующей симптоматики.
- повышение уровня ACT или АЛТ >5 ВГН в течение >2 недель после инъекции независимо от уровня общего билирубина или сопутствующей симптоматики.
- повышение уровня ACT или АЛТ >3 ВГН и уровня общего билирубина >2 ВГН.
- повышение уровня ACT или АЛТ >3 ВГН, сопровождающееся симптомами поражения печени (усталость, тошнота, рвота, боль или болезненность в верхнем правом квадранте живота, лихорадка или сыпь).
У пациента наблюдаются любые из перечисленных ниже лабораторных отклонений:
- абсолютное количество нейтрофилов <500 × 106/л (<500 /мм3).
- количество лимфоцитов по результатам двух последовательных анализов <500 × 106/л (<500 /мм3).
- количество тромбоцитов <50 × 109/л (<50000 /мм3 или <50000 × 106/л).
Подтверждённая беременность во время применения препарата Артлегиа (см. раздел «Применение при беременности и в период грудного вскармливания»).
Перфорация желудочно-кишечного тракта (см. раздел «Особые указания»).
Тяжёлая или угрожающая жизни инфекция (см. раздел «Особые указания»).
Применение у детей
Безопасность и эффективность препарата Артлегиа у детей и подростков младше 18 лет на данный момент не установлены. Данные по применению отсутствуют.
Режим дозирования:
Рекомендуемая доза составляет 64 мг 1 раз каждые 4 недели или 1 раз каждые 2 недели подкожно.
Особые группы пациентов
Пожилые пациенты (>65 лет): коррекция дозы не требуется.
Пациенты с почечной недостаточностью: безопасность и эффективность препарата Артлегиа у пациентов с почечной недостаточностью не изучалась. Данные по применению отсутствуют.
Пациенты с печёночной недостаточностью: безопасность и эффективность препарата Артлегиа у пациентов с печёночной недостаточностью не изучалась. Данные по применению отсутствуют.
Инструкция по подготовке к инъекции и введению препарата
Извлеките флакон с препаратом Артлегиа из холодильника заранее: следует подождать примерно 30 минут перед инъекцией, чтобы препарат нагрелся до комнатной температуры. Не подогревайте препарат.
Подготовьтесь к инъекции
Шаг 1
Вымойте руки тёплой водой с мылом, выберите ровную чистую поверхность, внимательно осмотрите флакон с препаратом и не используйте его, если:
- он был извлечён из холодильника более 4 часов назад,
- на нём указано неправильное название препарата,
- истёк срок годности, указанный на упаковке,
- на флаконе имеются трещины, повреждения или утечка препарата,
- раствор мутный, изменил цвет или содержит хлопья, или частицы.
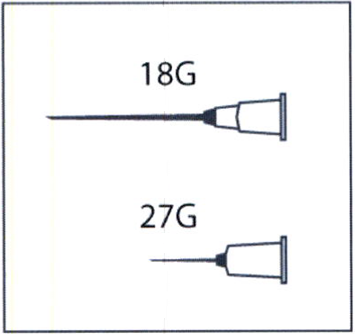
Приготовьте одноразовый шприц для подкожных инъекций вместимостью 1–2 мл, две одноразовых стерильных инъекционных иглы (рекомендуется использовать иглу размера 18G для набора препарата из флакона и иглу 27G для выполнения подкожной инъекции), 2 спиртовые и 1 стерильную салфетки.
Шаг 2
Наденьте на шприц более толстую иглу для набора препарата, не снимая защитный колпачок. Удалите пластмассовую защитную крышку с флакона, протрите резиновую пробку спиртовой салфеткой.
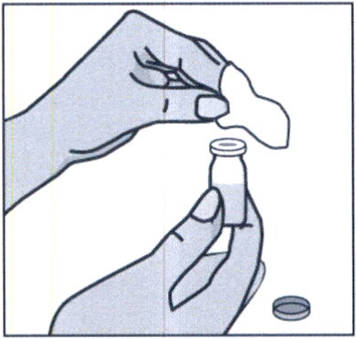
Возьмите шприц в правую руку, удалите колпачок с иглы шприца и введите иглу вертикально в центр пробки флакона так, чтобы кончик иглы появился с внутренней стороны пробки.
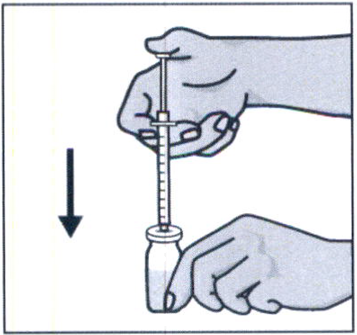
Удерживая правой рукой шприц, возьмите левой рукой флакон и переверните его так, чтобы вся жидкость собралась над пробкой. Оттягивая поршень шприца вниз, наберите в шприц все содержимое флакона.
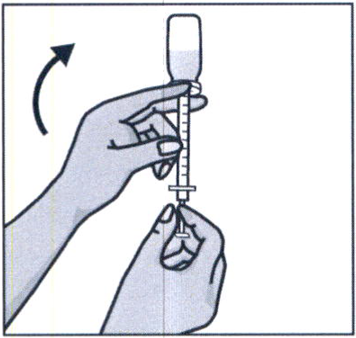
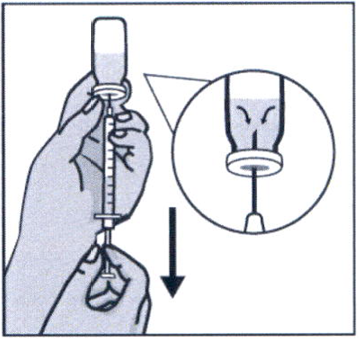
Вытащите иглу из флакона и закройте колпачком. Не снимая защитный колпачок замените на иглу для подкожных инъекций. Использованную иглу для набора препарата выбросьте в контейнер для острых предметов.
Внимание! Не выполняйте инъекцию иглой для набора препарата, это может привести к боли и повреждениям в месте инъекции.
Шаг 3
Осторожно снимите колпачок с иглы для подкожных инъекций. Не прикасайтесь к ней и соблюдайте осторожность чтобы не уколоться кончиком иглы. Удерживайте шприц вертикально и постучите по нему пальцем, чтобы пузырьки воздуха поднялись вверх. Удерживая шприц вертикально, медленно сдвиньте поршень чтобы изгнать из шприца воздух и избыточный объём жидкости так, чтобы поршень шприца остановился на отметке 0,4 мл.
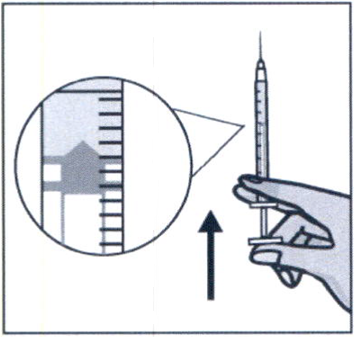
Выберите место для инъекции
Выберите место инъекции на верхней части бедра или на животе на расстоянии не менее 5 см от пупка. Если инъекции делает медицинский работник, то препарат можно вводить в другие места для подкожных инъекций. Не рекомендуется введение препарата в места родинок, шрамов, повреждений или уплотнений, покраснений, повышенной чувствительности кожных покровов.
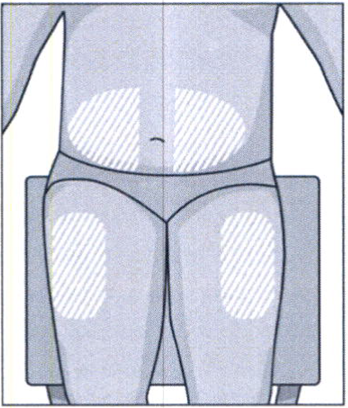
Рекомендуется регулярно менять место введения препарата. Новое место для инъекции должно находиться на расстоянии не менее 2,5 см от предыдущего места инъекции. При желании можно поочерёдно выполнять инъекции под кожу бёдер и живота.
Выполните инъекцию
Протрите кожу выбранного места инъекции новой спиртовой салфеткой. Позвольте месту инъекции высохнуть и не прикасайтесь к нему до инъекции.
Осторожно сожмите кожу вокруг обработанного места инъекции второстепенной рукой (например, если Вы правша, используйте левую руку) и плотно удерживайте её.
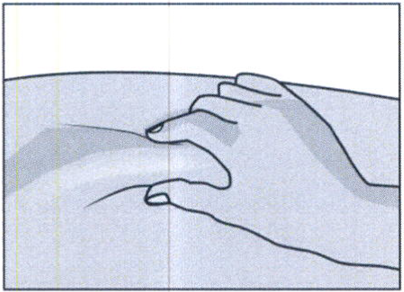
Удерживайте шприц в ведущей руке над приподнятым участком кожи под углом 90 градусов. Воткните иглу в кожу быстрым плавным толкающим движением. Если количество подкожного жира на брюшной стенке невелико, можно выполнять инъекцию под углом 45 градусов.
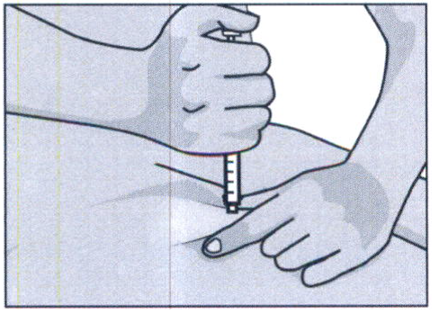
Не смещайте иглу относительно тканей и медленно нажимайте на поршень, пока весь объём препарата из шприца не будет введён под кожу. Поршень должен достичь дна шприца. Подождите несколько секунд перед извлечением иглы.
Извлеките иглу из кожи под тем же углом, под которым она была введена. В месте инъекции возможно небольшое кровотечение. При необходимости приложите стерильную салфетку на место инъекции.
Помните!
Выбрасывайте использованные шприцы в контейнер для острых предметов сразу после инъекции. Когда контейнер будет заполнен полностью, аккуратно и тщательно закройте его и выкиньте в мусорное ведро.
Всегда используйте новый шприц, не используйте повторно старые шприцы.
Побочные эффекты
Безопасность применения препарата Артлегиа оценивалась в двойном слепом рандомизированном клиническом исследовании CREDO1. Всего в исследовании участвовало 428 пациентов со среднетяжёлым и тяжёлым ревматоидным артритом с недостаточным контролем на терапии метотрексатом. 142 пациента получали олокизумаб в дозе 64 мг один раз каждые 2 недели (к2н), 143 пациента получали олокизумаб 64 мг один раз каждые 4 недели (к4н), 143 пациента получали плацебо. Все пациенты находились на фоновой терапии метотрексатом.
Наиболее часто встречающимися нежелательными реакциями были лейкопения, нейтропения, повышение уровня печёночных трансаминаз.
Перечень нежелательных реакций приведён в соответствии с системно-органными классами (СОК) MedDRA. В пределах каждого класса нежелательные реакции распределены по категориям частоты встречаемости: очень часто (>1/10), часто (от >1/100 до <1/10), нечасто (от >1/1 000 до <1/100), редко (от >1/10 000 до <1/1 000), очень редко (<1/10 000) и частота неизвестна.
| Класс частоты | |||
|---|---|---|---|
| Перечень СОК | Очень часто | Часто | Нечасто |
| Инфекции и паразитарные заболевания | бронхит | лёгочный туберкулёз, кандидоз кожи, вульвовагинальный кандидоз, отрубевидный лишай, подкожный абсцесс, рожистое воспаление, сепсис. вызванный стафилококковой инфекцией, синдром токсического шока | |
| Нарушения со стороны крови и лимфатической системы | лейкопения, нейтропения | эозинофилия | |
| Нарушения метаболизма и питания | гиперхолестеринемия | ||
| Нарушения со стороны печени и желчевыводящих путей | повышение уровня ACT, повышение уровня АЛТ | повышение уровня ГГТ | |
| Нарушения со стороны кожи и подкожных тканей | зуд, сыпь | изменение цвета пота, дерматит, экхимоз, зудящая сыпь | |
| Общие нарушения и реакции в месте введения | боль в месте инъекции, эритема | ||
| Лабораторные и инструментальные данные | позитивный тест на микобактерию туберкулёза | ||
Перфорации дивертикула
Несмотря на то, что у пациентов в исследовании CREDO1 не было выявлено нежелательных явлений со стороны желудочно-кишечного тракта (ЖКТ), связанных с применением олокизумаба, в продолжающихся клинических исследованиях, включающих в общей сложности более 2000 пациентов с ревматоидным артритом, были зарегистрированы случаи перфорации дивертикула, связанные с применением олокизумаба. Частота данной нежелательной реакции неизвестна. В связи с тем. что риск перфорации желудочно-кишечного тракта характерен для ингибиторов ИЛ-6, следует соблюдать осторожность при применении препарата у пациентов с факторами риска перфорации ЖКТ.
Реакции гиперчувствительности
В исследовании CREDO1 наблюдалось дозозависимое увеличение реакций гиперчувствительности в группах пациентов, получавших олокизумаб: доля пациентов, у которых в ходе лечения возникло хотя бы одно нежелательное явление, относящееся к реакциям гиперчувствительности, включая: зуд, сыпь, аллергический дерматит, повышение уровня эозинофилов в крови, составила 4,2 % в группе, получавшей олокизумаб к4н, 7,0 % в группе, получавшей олокизумаб к2н и 2,1 % в группе плацебо.
В продолжающихся клинических исследованиях был зарегистрирован случай анафилактической реакции на введение олокизумаба (частота неизвестна).
Инфекции
В исследовании CREDO1 инфекции встречались с приблизительно одинаковой частотой во всех терапевтических группах: 14,1 % в группе, получавшей олокизумаб 64 мг к4н, 15,4 % в группе, получавшей олокизумаб 64 мг к2н и 16,2 % в группе плацебо.
В группе пациентов, получавших олокизумаб 64 мг к2н. чаще развивались связанные с инфекциями серьёзные нежелательные явления (2,8 %) по сравнению с группой пациентов, получавших олокизумаб 64 мг к4н (0 %) и плацебо (1,4 %).
В группах пациентов, получавших олокизумаб, были зарегистрированы следующие случаи серьёзных инфекций, не встречавшихся в группе плацебо: подкожный абсцесс (2), лёгочный туберкулёз (1), сепсис, вызванный стафилококковой инфекцией (1), и синдром токсического шока (1).
Повышение уровня печёночных трансаминаз
В исследовании CREDO1 частота повышения АЛТ, расценённого исследователями как нежелательное явление, составляла 23,2 % в группе, получавшей олокизумаб 64 мг к4н, 17,5 % в группе, получавшей олокизумаб 64 мг к2н и 17,7 % в группе плацебо. Частота повышения ACT, расцененного исследователями как нежелательное явление, составляла 15,5 % в группе, получавшей олокизумаб к4н, 11,2 % группе, получавшей олокизумаб к2н и 7,0 % в группе плацебо.
В целом в течение периода терапии наблюдались колебания индивидуальных уровней АЛТ. Всего подъем уровня АЛТ выше верхней границы нормы (1 × ВГН) отмечался хотя бы один раз за период лечения (24 недели) приблизительно у 50 % пациентов, получавших олокизумаб и у 27 % пациентов, получавших плацебо (Таблица 4). Ни у кого из пациентов не отмечалось одновременного повышения АЛТ и ACT > З × ВГН с повышением билирубина > 2 × ВГН.
| Уровень АЛТ | Доля пациентов | |||||
|---|---|---|---|---|---|---|
| Исходный уровень | За период лечения* | |||||
| ОКЗ 64 мг к4н | ОКЗ 64 мг к2н | Плацебо | ОКЗ 64 мг к4н | ОКЗ 64 мг к2н | Плацебо | |
| >1 × ВГН <З × ВГН | 9,9 % | 8,4 % | 9,9 % | 52,9 % | 47,5 % | 27,0 % |
| >З × ВГН <5 × ВГН | 0 | 0 | 0 | 5,7 % | 6,4 % | 3,5 % |
| >5 × ВГН | 0 | 0,7 % | 0 | 5,7 % | 2,8 % | 1,4 % |
* учитывалось наибольшее значение АЛТ у каждого пациента за 24-недельный период лечения ВГН — верхняя граница нормы; ОКЗ – олокизумаб
Гиперлипидемия
В исследовании CREDO1 повышение уровня липидов крови на фоне лечения, расцененное исследователями как нежелательное явление, наблюдалось у 8,5 % пациентов в группе, получавшей олокизумаб 64 мг к4н, 8,4 % пациентов в группе, получавшей олокизумаб 64 мг к2н и 2,8 % пациентов в группе плацебо.
В среднем уровни общего холестерина, ЛПНП и ЛПВП возрастали в группах пациентов, получавших олокизумаб, в течение первых 4 недель терапии. Затем в группе, получавшей олокизумаб 64 мг к2н, средние уровни липидов снижались и к концу периода лечения возвращались к значениям в группе плацебо, тогда как у пациентов, получавших олокизумаб 64 мг к4н, высокие средние уровни липидов в крови сохранялись до конца периода лечения.
Нейтропения
В исследовании CREDO1 среднее абсолютное число нейтрофилов через 12 недель терапии снизилось в группах, получавших олокизумаб, по сравнению с плацебо и затем оставалось стабильным до конца периода лечения (Таблица 5).
| Длительность лечения | Препарат и доза | ||
|---|---|---|---|
| ОКЗ 64 мг к4н | ОКЗ 64 мг к2н | Плацебо | |
| 0 | 5,9 × 109 /л | 5,2 × 109 /л | 5,7 × 109 /л |
| 12 недель | 3,9 × 109 /л | 3,4 × 109 /л | 5,6 × 109 /л |
| 24 недели | 3,7 × 109 /л | 3,2 × 109 /л | 5,З × 109/л |
Соответственно доля пациентов, у которых хотя бы один раз в ходе лечения регистрировалось такое нежелательное явление, как нейтропения, составляла 11,2 % пациентов в группе, получавшей олокизумаб 64 мг к4н, 7,7 % пациентов в группе, получавшей олокизумаб 64 мг к2н и 3,5 % пациентов в группе плацебо.
Передозировка
В клинических исследованиях случаев передозировки не наблюдалось. Однако дополнительные клинические данные показывают, что общий профиль безопасности олокизумаба у пациентов, получавших препарат в дозе 240 мг к2н (480 мг в месяц) в течение 12 недель сопоставим с общим профилем безопасности у пациентов, получавших препарат в рекомендованной дозе.
Дети
Данные о передозировке у детей отсутствуют.
Взаимодействие
Одновременное применение с метотрексатом не влияло на экспозицию олокизумаба. Не ожидается также влияния олокизумаба на экспозицию метотрексата при их одновременном применении, клинические данные отсутствуют. Во всех клинических исследованиях у пациентов с ревматоидным артритом олокизумаб применялся совместно с метотрексатом.
Специальные клинические исследования лекарственных взаимодействий олокизумаба не проводились. По результатам клинического исследования CREDO1 не сообщалось о случаях клинически значимых лекарственных взаимодействий олокизумаба с другими препаратами.
В исследовании in vitro на криоконсервированных гепатоцитах человека олокизумаб обращал ингибиторный эффект ИЛ-6 на активность CYP1A1/2, 2B6, 2C9, ЗA4/5 и 2C19. а также на активность NTCP. Таким образом, следует принимать во внимание, что у пациентов с активным ревматоидным артритом может потребоваться коррекция доз препаратов, метаболизируемых данными изоформами CYP, после начала применения препарата Артлегиа.
Концентрация следующих препаратов может снизиться при совместном применении с препаратом Артлегиа (список не является исчерпывающим): статины (симвастатин, ловастатин, аторвастатин); оральные контрацептивы; блокаторы кальциевых каналов; глюкокортикоиды (дексаметазон, метилпреднизолон); варфарин; хинидин; теофиллин; тизанидин; фенитоин; пимозид; циклоспорин; сиролимус; такролимус; бензодиазепины (например, диазепам, алпразолам, триазолам, мидазолам, бромазепам).
Особые указания
Назначать лечение препаратом Артлегиа и наблюдать за ходом лечения разрешается врачам, имеющим опыт в диагностике и лечении ревматоидного артрита.
Анафилактические или анафилактоидные реакции: введение препаратов, содержащих белки, может быть связано с возникновением иммунологических/аллергических или неиммунологических реакций повышенной чувствительности к препарату, которые могут быть тяжёлыми. Эти реакции могут возникать в виде острой инфузионной реакции, аллергической реакции или реакции гиперчувствительности замедленного типа. Таким образом, первое введение препарата Артлегиа следует выполнять в медицинском учреждении, где имеются лекарственные средства и оборудование для купирования анафилактических и анафилактоидных реакций. В клинических исследованиях был отмечен случай серьёзной анафилактической реакции на введение препарата Артлегиа.
Инфекции: для пациентов, получающих иммуносупрессивные препараты, включая блокаторы сигнального пути ИЛ-6, характерна повышенная частота развития инфекций.
Применение препарата Артлегиа связано с повышенным риском развития или активизациией инфекций. Не следует начинать терапию препаратом Артлегиа пациентам с инфекциями в активной фазе. Следует с осторожностью проводить лечение препаратом Артлегиа пациентов, имеющих факторы риска развития инфекций. При развитии серьёзных инфекций терапию препаратом Артлегиа следует прекратить. Пациентов следует проинструктировать о возможных признаках и симптомах развития инфекции, требующих немедленного обращения к врачу.
Туберкулёзная инфекция: перед началом терапии препаратом Артлегиа необходимо провести обследование пациента на наличие латентной формы туберкулёзной инфекции.
Пациентам с выявленной латентной формой туберкулёзной инфекции перед началом терапии препаратом Артлегиа следует провести стандартный курс противотуберкулёзной терапии.
Следует с осторожностью назначать препарат Артлегиа пациентам, находящимся в тесном контакте (совместное проживание или нахождение в других замкнутых пространствах, например, на рабочем месте, на общественных собраниях или в здании на протяжении длительных периодов в течение дня) с лицом, страдающим активным туберкулёзом. Перед применением препарата Артлегиа у таких пациентов следует тщательно оценить соотношение риска и пользы применения препарата.
Риск перфорации желудочно-кишечного тракта: при применении ингибиторов сигнального пути ИЛ-6 известны случаи перфорации желудочно-кишечного тракта, в основном на фоне дивертикулита. Следует соблюдать осторожность при применении препарата Артлегиа у пациентов с дивертикулитом или перфорацией кишечника в анамнезе и другими факторами риска перфорации кишечника. При появлении желудочно-кишечных симптомов, таких как абдоминальная боль, на фоне лечения препаратом Артлегиа, следует незамедлительно провести обследование пациента.
Почечная недостаточность: пациентов с почечной недостаточностью не включали в клиническое исследование препарата Артлегиа. В связи с отсутствием данных следует соблюдать осторожность при применении препарата Артлегиа у пациентов с нарушениями функции почек.
Нарушения функции печени: применение препарата Артлегиа так же, как и других ингибиторов ИЛ-6, связано с повышением уровня АЛТ, ACT и гамма-глутамил грансферазы (см. раздел «Повышение уровня печёночных трансаминаз»). Пациентов с уровнем АЛТ или ACT >1,5 × ВГН не включали в клиническое исследование. Следует соблюдать осторожность при применении препарата Артлегиа у пациентов с нарушениями функции печени и печёночной недостаточностью.
Мониторинг лабораторных показателей крови: в клинических исследованиях было зарегистрировано снижение абсолютного числа нейтрофилов и лейкоцитов на фоне лечения препаратом Артлегиа и другими ингибиторами ИЛ-6. По данным применения других ингибиторов ИЛ-6, нейтропения на фоне лечения не приводила к повышению частоты инфекций.
Пациентов с уровнем лейкоцитов <3,5 × 109/л, уровнем нейтрофилов <2000 × 106/л (<2000/мм3) не включали в клиническое исследование.
Вакцинация: безопасность иммунизации живыми вакцинами на фоне применения ингибиторов ИЛ-6, в том числе олокизумаба, не установлена. Пациентов с необходимостью вакцинации живыми вакцинами не включали в клиническое исследование.
Злокачественные новообразования: данные о безопасности применения олокизумаба у пациентов со злокачественными новообразованиями отсутствуют, риск развития злокачественных опухолей на фоне терапии препаратом Артлегиа не известен.
Влияние на способность управлять транспортными средствами или работать с механизмами
Исследования по изучению влияния препарата на способность управлять транспортными средствами и механизмами не проводились. Хотя на данный момент при терапии олокизумабом нежелательные реакции, связанные с головокружением, не отмечались, головокружение часто наблюдалось при терапии другими ингибиторами ИЛ-6. Пациентам, испытывающим головокружение во время терапии препаратом Артлегиа, следует рекомендовать не управлять транспортными средствами и механизмами до тех пор. пока головокружение не прекратится.
Форма выпуска
Раствор для подкожного введения, 160 мг/мл.
Хранение
В защищённом от света месте при температуре от 2 до 8 °C.
Хранить в недоступном для детей месте.
Не замораживать.
Срок годности
3 года.
Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
Отпускают по рецепту
Классификация
-
Фармакотерапевтическая группа
-
АТХ
-
Действующее вещество
Подробнее по теме
Ознакомьтесь с дополнительными сведениями о препарате Артлегиа:
