ПланиЖенс® дезо 30
Лекарственная форма
таблетки
Состав
1 таблетка содержит:
действующие вещества: дезогестрел — 150 мкг, этинилэстрадиол — 30 мкг;
вспомогательные вещества: мальтитол — 30,00 мг, крахмал кукурузный — 8,00 мг, кремния диоксид коллоидный — 0,75 мг, коповидон — 3,00 мг, бутилгидрокситолуол — 0,07 мг, натрия стеарилфумарат — 1,20 мг, макрогол 4000 — 1,80 мг, целлюлоза микрокристаллическая (тип 200) — 35,00 мг.
Описание
Круглые плоскоцилиндрические таблетки белого или почти белого цвета, с фаской.
Фармакологическое действие
Фармакодинамика
Контрацептивный эффект комбинированных (эстроген+гестаген) пероральных контрацептивных препаратов (КОК) основан на взаимодействии различных факторов, самыми важными из которых являются подавление овуляции и повышение вязкости секрета шейки матки, препятствующее проникновению сперматозоидов в полость матки. Препарат ПланиЖенс® дезо 30 представляет собой монофазный низкодозированный КОК, содержащий комбинацию дезогестрела и этинилэстрадиола. Дезогестрел — синтетический прогестаген, обладающий сильной ингибирующей овуляцию активностью. Этинилэстрадиол является хорошо известным синтетическим эстрогеном. При правильном применении индекс Перля (ИП — показатель, отражающий частоту наступления беременности у 100 женщин в течение 1 года применения контрацептива) составляет менее 1: в крупном многоцентровом исследовании эффективности контрацепции комбинацией дезогестрел + этинилэстрадиол (количество циклов — 23258) нескорректированный ИП составил 0,1. При неправильном применении, в том числе при пропуске своевременного приёма таблеток, ИП может возрастать. У женщин, принимающих КОК, цикл становится более регулярным, уменьшаются болезненность и интенсивность менструальноподобных кровотечений, в результате чего снижается риск железодефицитной анемии.
Фармакокинетика
Дезогестрел
Всасывание
Дезогестрел после перорального приёма быстро и полностью всасывается, превращаясь затем в этоногестрел (3-кето-дезогестрел). Максимальная концентрация этоногестрела (Сmax) в плазме крови (2 нг/мл) достигается через 1,5 часа. Биодоступность этоногестрела составляет 62–81 %.
Распределение
Этоногестрел связывается с альбумином плазмы крови и с глобулином, связывающим половые гормоны (ГСПГ). Только 2–4 % от общей концентрации этоногестрела присутствуют в плазме крови в свободном виде, 40–70 % специфически связываются с ГСПГ. Увеличение концентрации ГСПГ, вызванное этинилэстрадиолом, оказывает влияние на распределение между белками крови, приводя к увеличению ГСПГ — связанной фракции и уменьшению фракции, связанной с альбумином. Кажущийся объём распределения дезогестрела составляет 1,5 л/кг.
Метаболизм
Этоногестрел полностью метаболизируется по известным путям метаболизма половых гормонов (сульфатирование и глюкуронидация). Скорость клиренса из плазмы крови составляет 2 мл/мин/кг. Взаимодействия этоногестрела и этинилэстрадиола при одновременном приёме не выявлено.
Выведение
Концентрация этоногестрела в плазме крови уменьшается в 2 фазы. Заключительная стадия характеризуется периодом полувыведения (T½), составляющим около 30 часов. Дезогестрел и его метаболиты выводятся почками и через кишечник в соотношении примерно 6:4.
Условия равновесного состояния
На фармакокинетику этоногестрела оказывает влияние ГСПГ, концентрация которого возрастает под действием этинилэстрадиола в 3 раза. При ежедневном приёме концентрация этоногестрела в плазме крови увеличивается в 2–3 раза в течение 3–13 дней, достигая постоянного значения во второй половине цикла приёма препарата.
Этинилэстрадиол
Всасывание
Этинилэстрадиол после перорального приёма быстро и полностью всасывается. Его максимальная концентрация в плазме крови достигается в течение 1–2 часов после приёма. Абсолютная биодоступность (результат пресистемного метаболизма) составляет около 60 %.
Распределение
Этинилэстрадиол неспецифически связывается с альбумином плазмы крови практически полностью (98,5 %) и способствует увеличению концентрации ГСПГ. Кажущийся объём распределения этинилэстрадиола составляет 5 л/кг.
Метаболизм
Этинилэстрадиол подвергается пресистемному метаболизму как в слизистой оболочке тонкой кишки, так и в печени. Этинилэстрадиол первоначально метаболизируется в ходе ароматического гидроксилирования с образованием разнообразных гидроксилированных и метилированных метаболитов, которые присутствуют как в свободном состоянии, так и в виде конъюгатов с глюкуронидами и сульфатами. Скорость клиренса этинилэстрадиола из плазмы крови составляет около 5 мл/мин/кг.
Выведение
Концентрация этинилэстрадиола в плазме крови уменьшается в 2 фазы. Заключительная фаза характеризуется Т½ около 24 часов. В неизменённом виде препарат не выводится, метаболиты этинилэстрадиола экскретируются почками и через кишечник в соотношении 4:6. Т½ метаболитов составляет около суток.
Условия равновесного состояния
Равновесная концентрация достигается после 3–4 дней приёма, когда концентрация в плазме крови на 30–40 % превышает концентрацию после приёма одной дозы.
Показания
Пероральная контрацепция.
Противопоказания
Применение препарата ПланиЖенс® дезо 30, как и других КОК, противопоказано при наличии любого из нижеперечисленных заболеваний/состояний или факторов риска:
- Венозный тромбоз или тромбоэмболия (ВТЭ), в том числе, тромбоз глубоких вен (ТГВ), тромбоэмболия лёгочной артерии (ТЭЛА), в настоящее время или в анамнезе.
- Артериальный тромбоз или тромбоэмболия (АТЭ), в том числе инфаркт миокарда, инсульт или продромальные состояния (в том числе, транзиторная ишемическая атака, стенокардия), в настоящее время или в анамнезе.
- Выявленная наследственная или приобретённая предрасположенность к ВТЭ или АТЭ, включая резистентность к активированному протеину С, гипергомоцистеинемию, дефицит антитромбина III, дефицит протеина С, дефицит протеина S, антифосфолипидные антитела (антитела к кардиолипину, волчаночный антикоагулянт).
- Наличие множественных факторов высокого риска развития ВТЭ или АТЭ (см. раздел «Особые указания») или одного серьёзного фактора риска, такого как:
- сахарный диабет с диабетической ангиопатией;
- тяжёлая дислипопротеинемия;
- неконтролируемая артериальная гипертензия (артериальное давление 160/100 мм рт.ст. и выше.
- Мигрень с очаговой неврологической симптоматикой в анамнезе.
- Обширное оперативное вмешательство с длительной иммобилизацией.
- Панкреатит, сопровождающийся выраженной гипертриглицеридемией (в т.ч. в анамнезе).
- Тяжёлые заболевания печени в настоящее время или в анамнезе (до нормализации показателей функции печени).
- Опухоли печени (доброкачественные и злокачественные), в том числе в анамнезе.
- Гормонозависимые злокачественные новообразования половых органов или молочной железы (в том числе подозрение на них).
- Гиперплазия эндометрия.
- Кровотечение из влагалища неясной этиологии.
- Беременность (в том числе предполагаемая).
- Период грудного вскармливания.
- Гиперчувствительность к дезогестрелу и/или этинилэстрадиолу, или к любому из вспомогательных веществ в составе препарата.
- Возраст до 18 лет (в связи с отсутствием данных по эффективности и безопасности применения комбинации дезогестрел+этинилэстрадиол у девочек-подростков в возрасте до 18 лет).
- Совместное применение с противовирусными препаратами прямого действия, содержащими омбитасвир/паритапревир/ритонавир и дасабувир (см. разделы «Взаимодействие с другими лекарственными средствами» и «Особые указания»).
- Непереносимость фруктозы, дефицит сахаразы/изомальтазы, синдром глюкозо-галактозной мальабсорбции.
При возникновении любого из данных заболеваний/состояний или факторов риска на фоне применения контрацептива, приём препарата следует немедленно прекратить.
С осторожностью
Если какие-либо из состояний/заболеваний или факторов риска, указанных ниже, имеются в настоящее время, следует провести тщательную оценку ожидаемой пользы к возможному риску применения препарата ПланиЖенс® дезо 30 для каждой женщины индивидуально и обсудить это до начала приёма препарата:
- факторы риска развития тромбоза и тромбоэмболий (курение, возраст, наличие в семейном анамнезе венозного или артериального тромбоза/тромбоэмболии или предрасположенность к тромбозам у кого-либо из ближайших родственников — родителей, сестёр или братьев — в возрасте менее 50 лет), ожирение, дислипопротеинемия, контролируемая артериальная гипертензия, мигрень без очаговой неврологической симптоматики, неосложнённые заболевания клапанов сердца);
- варикозное расширение вен, поверхностный тромбофлебит;
- сахарный диабет без сосудистых нарушений;
- системная красная волчанка;
- гемолитико-уремический синдром;
- хронические воспалительные заболевания кишечника (болезнь Крона или язвенный колит);
- серповидно-клеточная анемия;
- гипертриглицеридемия (в том числе в семейном анамнезе);
- острые и хронические заболевания печени, в том числе врождённые гипербилирубинемии (при нормальных показателях функций печени);
- послеродовый период.
Беременность и лактация
Беременность
Приём комбинации дезогестрел+этинилэстрадиол в период беременности противопоказан. В случае диагностирования беременности на фоне применения препарата ПланиЖенс® дезо 30 следует немедленно прекратить его приём. Многочисленные эпидемиологические исследования не выявили ни увеличения риска возникновения дефектов развития у детей, рождённых женщинами, получавшими половые гормоны до беременности, ни наличия тератогенного действия, когда половые гормоны принимались по неосторожности в ранние сроки беременности.
Период грудного вскармливания
Применение препарата ПланиЖенс® дезо 30, как и других КОК, может уменьшать количество грудного молока и изменять его состав, поэтому приём препарата противопоказан до прекращения грудного вскармливания.
Способ применения и дозы
Календарная упаковка содержит 21 таблетку. Упаковка также содержит блок наклеек, состоящий из 7 самоклеящихся полосок с отмеченными на них названиями дней недели, необходимый для оформления календаря приёма. Необходимо выбрать полоску, где первым указан тот день недели, в который начинается приём таблеток. Например, если начало приёма таблеток приходится на среду, следует использовать полоску, которая начинается со «Ср.» (рис. 1).

Полоску наклеивают вдоль верхней части упаковки так, чтобы обозначение первого дня находилось над той таблеткой, на которую направлена стрелка с надписью «Старт» (рис. 2).
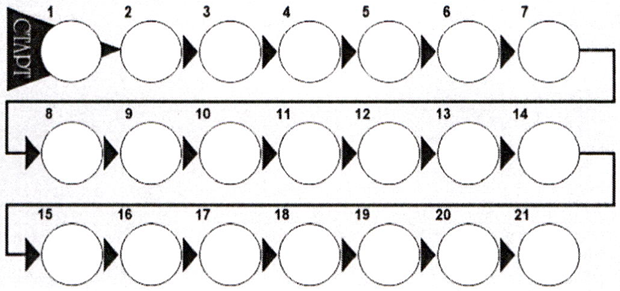
Теперь видно, в какой день недели следует принять каждую таблетку (рис. 3)
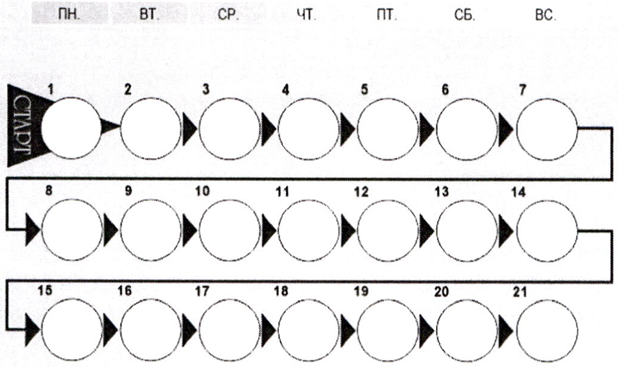
Таблетки необходимо принимать внутрь, ежедневно в одно и то же время, не разжёвывая, запивая небольшим количеством воды. Следуя направлению стрелок, принимайте ПланиЖенс® дезо 30 в течение 21 дня. Приём следующей упаковки необходимо начинать на 8-ой день после 7-дневного перерыва, во время которого обычно развивается менструальноподобное кровотечение (кровотечение «отмены»). Как правило, оно начинается на 2–3 день после приёма последней таблетки контрацептива и может не закончиться до начала приёма таблеток из нового блистера. Приём таблеток из новой упаковки следует начинать в один и тот же день недели, соответственно кровотечение «отмены» будет каждый месяц примерно в одно и то же время.
Начало приёма препарата
Если гормональные контрацептивы не применялись в течение предыдущего месяца
Приём таблеток следует начинать в 1 день менструального цикла (т.е. в 1-й день менструального кровотечения). Допускается начало приёма препарата на 2–5 день цикла, но в таком случае следует использовать дополнительный (барьерный) метод контрацепции в течение первых 7 дней приёма таблеток в первом цикле.
При переходе с других комбинированных гормональных контрацептивных препаратов (КОК, вагинального кольца или трансдермального пластыря)
Предпочтительнее начинать приём препарата ПланиЖенс® дезо 30 на следующий день после приёма последней таблетки ранее применяемого КОК, содержащей гормоны, но не позднее следующего дня после обычного 7-дневного перерыва (если женщина принимала КОК, содержащий 21 таблетку в упаковке) или после приёма последней не содержащей гормонов таблетки (если женщина принимала КОК, содержащий 28 таблеток в упаковке). Приём препарата следует начинать в день удаления вагинального кольца или пластыря, но не позднее дня, когда должно быть введено новое кольцо или наклеен новый пластырь. Ни в коем случае не следует превышать рекомендуемый безгормональный интервал предыдущего метода контрацепции.
Переход с контрацептивов, содержащих только прогестаген («мини-пили», инъекционные формы, имплантат), или с прогестаген-высвобождающей внутриматочной системы (ВМС)
При приёме «мини-пили» перейти на приём препарата ПланиЖенс® дезо 30 можно в любой день; при применении имплантата или ВМС — в день их удаления; при применении инъекционного контрацептива — в день, когда должна быть сделана следующая инъекция. Во всех случаях необходимо использовать дополнительно барьерный метод контрацепции в течение первых 7 дней приёма препарата ПланиЖенс® дезо 30.
После аборта, в том числе самопроизвольного, в I триместре беременности
Можно начинать приём препарата немедленно. В этом случае нет необходимости в дополнительных методах контрацепции.
После родов или прерывания беременности (в том числе самопроизвольного) во Ⅱ триместре беременности
Для кормящих женщин см. раздел «Применение во время беременности и в период грудного вскармливания».
Рекомендуется начинать приём препарата не ранее 21–28 дня после родов (при отсутствии или прекращении грудного вскармливания) или аборта во II триместре беременности. Если приём начат позднее, необходимо использовать дополнительно барьерный метод контрацепции в течение первых 7 дней приёма препарата ПланиЖенс® дезо 30. Однако если после родов или аборта до начала приёма КОК у женщины уже были половые контакты, необходимо исключить беременность или дождаться первой менструации. При возобновлении применения препарата ПланиЖенс® дезо 30 необходимо принимать во внимание повышение риска развития ВТЭ в послеродовом периоде (см. раздел «Особые указания»).
Рекомендации в случае пропуска приёма препарата
Если опоздание в приёме препарата составило менее 12 часов, контрацептивная защита не снижается. Принять таблетку следует как можно скорее, следующая таблетка принимается в обычное время.
Если опоздание в приёме препарата составило более 12 часов, контрацептивная защита может быть снижена. При этом можно руководствоваться следующими двумя основными правилами:
- Приём препарата никогда не должен быть прерван более чем на 7 дней;
- Для достижения адекватного подавления гипоталамо-гипофизарно-яичниковой системы требуется 7 дней непрерывного приёма таблеток.
Цикличность приёма препарата подразумевает 3 недели применения. Соответственно можно дать следующие рекомендации:
Первая неделя приёма препарата
Необходимо принять последнюю пропущенную таблетку как можно скорее, как только женщина вспомнит об этом (даже если для этого нужно принять 2 таблетки одновременно). Следующую таблетку принимают в обычное время. Дополнительно должен быть использован барьерный метод контрацепции (например, презерватив) в течение следующих 7 дней. Если половой контакт имел место в течение недели перед пропуском таблетки, необходимо учитывать вероятность наступления беременности. Чем больше таблеток пропущено и чем ближе перерыв в приёме препарата к моменту полового контакта, тем выше риск беременности.
Вторая неделя приёма препарата
Необходимо принять последнюю пропущенную таблетку как можно скорее, как только женщина вспомнит об этом (даже если для этого нужно принять 2 таблетки одновременно).
Следующую таблетку принимают в обычное время. При условии, что женщина принимала таблетки правильно в течение 7 дней, предшествующих первой пропущенной таблетке, нет необходимости в использовании дополнительных (негормональных) методов контрацепции. В противном случае, а также при пропуске больше чем 1 таблетки, необходимо использовать дополнительные методы контрацепции в течение следующих 7 дней.
Третья неделя приёма препарата
Риск снижения надёжности контрацепции возрастает из-за предстоящего перерыва в приёме препарата. Если женщина принимала таблетки вовремя в течение 7 дней, предшествующих первой пропущенной таблетке, необходимости в использовании дополнительных мер контрацепции нет. Если в течение 7 дней, предшествующих первой пропущенной таблетке, были нарушения приёма препарата, то в течение последующих 7 дней необходимо дополнительно использовать барьерный метод контрацепции (например, презерватив) и в этом случае следует придерживаться какой-либо из указанных ниже рекомендаций:
- Необходимо принять последнюю пропущенную таблетку как можно скорее, как только женщина вспомнит об этом (даже если это означает приём 2-х таблеток одновременно). Далее таблетки принимают в обычное время, пока не закончатся таблетки из текущей упаковки. Приём таблеток из нового блистера следует начинать сразу же без обычного 7-дневного перерыва. Кровотечение «отмены» маловероятно, пока не закончатся таблетки из нового блистера, но могут отмечаться «мажущие» кровянистые выделения и/или «прорывные» кровотечения в дни приёма препарата.
- Можно также прервать приём таблеток из текущей упаковки, сделать перерыв на 7 или менее дней (включая дни пропуска таблеток), после чего начинать приём таблеток из нового блистера.
Не следует принимать более 2 таблеток в сутки!
Если женщина пропустила приём таблеток и затем во время перерыва в приёме препарата у неё нет кровотечения «отмены», необходимо исключить беременность.
Рекомендации в случае возникновения желудочно-кишечных расстройств
В случае тяжёлых желудочно-кишечных расстройств (рвота, диарея) всасывание препарата может быть неполным, поэтому следует принять дополнительные меры контрацепции. Если рвота возникает в течение 3–4 часов после приёма препарата, следует придерживаться рекомендаций, касающихся пропуска очередного приёма препарата. Если женщина не хочет менять свою обычную схему приёма, то она должна принять дополнительную таблетку (или таблетки) из другой упаковки.
Применение препарата в особых клинических группах
У детей и подростков
Безопасность и эффективность комбинации дезогестрел+этинилэстрадиол у девочек- подростков до 18 лет не изучались.
Изменение дня начала менструальноподобного кровотечения
Для того чтобы отсрочить начало менструальноподобного кровотечения, необходимо продолжить дальнейший приём таблеток из новой упаковки препарата ПланиЖенс® дезо 30 без 7-дневного перерыва. Отсрочить менструальноподобное кровотечение можно на любой срок до окончания таблеток из второй упаковки. На фоне приёма препарата из второй упаковки возможны «мажущие» или обильные кровянистые выделения. Возобновить регулярный приём препарата из очередной упаковки следует после обычного 7-дневного перерыва.
Для того чтобы перенести начало менструальноподобного кровотечения на другой день недели, следует сократить ближайший перерыв в приёме таблеток на желаемое количество дней. Чем короче перерыв, тем выше риск отсутствия кровотечения «отмены» в перерыве и возникновения «мажущих» или обильных кровянистых выделений во время приёма таблеток из второй упаковки (как и в случае отсроченного наступления менструальноподобного кровотечения).
Побочные эффекты
Возможные нежелательные реакции при применении комбинации дезогестрел+этинилэстрадиол распределены по системно-органным классам, с указанием частоты их возникновения согласно рекомендациям ВОЗ: часто (≥1/100 до <1/10), нечасто (≥1/1 000 до <1/100), редко (≥1/10 000 до <1/1 000).
Системно-органный класс | Часто | Нечасто | Редко |
Нарушения со стороны иммунной системы |
|
| Гиперчувствительность |
Нарушения со стороны обмена веществ и питания |
| Задержка жидкости |
|
Нарушения психики | Депрессия, смена настроения | Снижение либидо | Повышение либидо |
Нарушения со стороны нервной системы | Головная боль | Мигрень |
|
Нарушения со стороны органа зрения |
|
| Непереносимость контактных линз |
Нарушения со стороны сосудов |
|
| Венозная тромбоэмболия1, |
|
|
| артериальная тромбоэмболия1 |
Нарушения со стороны желудочно-кишечного тракта | Тошнота, боль в животе | Рвота, диарея |
|
Нарушения со стороны кожи и подкожных тканей |
| Кожная сыпь, крапивница | Узловатая эритема, многоформная эритема |
Нарушения со стороны репродуктивной системы и молочных желёз | Боль в груди, чувствительность молочных желёз | Увеличение молочных желёз | Выделения из влагалища, выделения из молочных желёз |
Лабораторные и инструментальные данные | Увеличение массы тела |
| Снижение массы тела |
1 — Количество случаев по данным наблюдательных когортных исследований: ≥1/10 000 — <1/1 000 женщин-лет (ЖЛ).
Нежелательные реакции, которые отмечались у женщин при приёме КОК, подробно описаны в разделе «Особые указания» и включают: венозные и артериальные тромбоэмболии, повышение артериального давления, гормонозависимые опухоли (например, опухоли печени, рак молочной железы), хлоазму.
Передозировка
Какие-либо серьёзные осложнения при передозировке комбинации дезогестрел + этинилэстрадиол не наблюдались.
Симптомы: тошнота, рвота, у девочек-подростков при случайном приёме — кровянистые выделения из влагалища.
Лечение: специфических антидотов не существует, следует проводить симптоматическую терапию.
Взаимодействие
Для определения возможного взаимодействия необходимо ознакомиться с инструкцией по применению сопутствующих препаратов. Взаимодействие КОК с другими лекарственными средствами может привести к «прорывным» кровотечениям и/или неэффективности пероральных контрацептивов. В литературе описаны следующие взаимодействия.
Печёночный метаболизм: возможно взаимодействие с лекарственными или растительными препаратами — индукторами микросомальных ферментов печени, прежде всего ферментов цитохрома Р450 (CYP), что может привести к увеличенному клиренсу и уменьшению концентрации половых гормонов в плазме крови, и соответственно к снижению эффективности КОК, в том числе и лекарственного препарата ПланиЖенс® дезо 30. К таким лекарственным препаратам относятся препараты, содержащие фенитоин, фенобарбитал, примидон, бозентан, карбамазепин, рифампицин; а также, возможно, окскарбазепин, топирамат, фелбамат, гризеофульвин; некоторые ингибиторы протеазы ВИЧ (например, ритонавир) и ненуклеозидные ингибиторы обратной транскриптазы (например, эфавиренз); растительные препараты, содержащие зверобой продырявленный (Hypericum perforatum). Индуцирование ферментов может происходить через несколько дней после сопутствующего применения. Максимальное индуцирование ферментов обычно наблюдается в течение нескольких недель. Индуцирование может сохраняться в течение 4 недель после отмены терапии препаратами-индукторами.
При совместном применении с гормональными контрацептивами многие комбинации ингибиторов протеазы ВИЧ (например, нелфинавира) и ненуклеозидных ингибиторов обратной транскриптазы (например, невирапина) и/или комбинации с препаратами для лечения вирусного гепатита С (например, боцепревиром, телапревиром) могут увеличить или уменьшить концентрацию в плазме прогестагена включая этоногестрел — активный метаболит дезогестрела, или эстрогена. В некоторых случаях суммарный эффект этих изменений может быть клинически значимым.
Женщинам, которые принимает любой из вышеуказанных лекарственных или растительных препаратов, индуцирующих микросомальные печёночные ферменты, следует информировать о возможном снижении эффективности контрацептива. При краткосрочной терапии препаратами-индукторами в течение всего периода их совместного применения и в течение 28 дней после окончания терапии в дополнение к приёму контрацептива дезогестрел+этинилэстрадиол следует использовать барьерные методы контрацепции (например, презерватив).
Если применение сопутствующего препарата-индуктора продолжается после окончания таблеток в текущей упаковке КОК, то приём КОК из следующей упаковки следует начинать сразу же, без обычного 7-дневного перерыва в приёме таблеток.
При длительной терапии лекарственными препаратами-индукторами целесообразно рассмотреть вопрос о выборе альтернативного метода контрацепции, не зависящего от влияния лекарственных препаратов-индукторов.
Совместное применение сильных (например, кетоконазола, итраконазола, кларитромицина) или средней активности (например, флуконазола, дилтиазема, эритромицина) ингибиторов CYP3A4 может увеличивать концентрацию эстрогена или прогестагена в плазме крови, в том числе и этоногестрела.
Было показано, что дозы эторикоксиба от 60 до 120 мг/сутки при совместном применении с КОК, содержащими 0,035 мг этинилэстрадиола, повышают концентрацию этинилэстрадиола в плазме крови в 1,4–1,6 раз, соответственно.
Пероральные контрацептивы могут влиять на метаболизм других лекарственных средств. Соответственно, концентрации лекарственных препаратов в плазме крови может повышаться (например, циклоспорина) или снижаться (например, ламотриджина).
Данные клинических исследований показывают, что этинилэстрадиол подавляет клиренс субстратов изофермента CYP1A2, приводя к небольшому (например, теофиллин) или умеренному (например, тизанидин) увеличению их концентраций в плазме крови.
Одновременный приём комбинации дезогестрел+этинилэстрадиол с лекарственными препаратами, содержащими омбитасвир/паритапревир/ритонавир и дасабувир, с рибавирином или без него, может увеличивать риск повышения активности АЛТ. Женщины, получающие препарат ПланиЖенс® дезо 30, должны перейти на альтернативный метод контрацепции (только прогестагенами или негормональными методами контрацепции).
Приём препарата ПланиЖенс® дезо 30 должен быть прекращён до начала проведения противовирусной терапии и может быть возобновлён не ранее чем через 2 недели после завершения терапии комбинацией данных противовирусных препаратов.
Особые указания
Если какие-либо из состояний/заболеваний или факторов риска, указанных ниже, имеются в настоящее время, то следует тщательно взвесить потенциальный риск и ожидаемую пользу применения КОК, в том числе комбинации дезогестрел + этинилэстрадиол в каждом индивидуальном случае и обсудить его с женщиной до начала приёма препарата. В случае ухудшения, утяжеления или первого проявления любого из этих состояний, заболеваний или факторов риска, женщина должна проконсультироваться со своим врачом для решения вопроса о прекращении приёма препарата.
Риск развития ВТЭ и АТЭ
В ходе эпидемиологических исследований была установлена связь между применением КОК и увеличением риска развития артериальных и венозных тромбозов и тромбоэмболий, таких как инфаркт миокарда, инсульт, ТГВ и ТЭЛА. Данные заболевания наблюдаются крайне редко.
Применение любого КОК связано с повышенным риском развития ВТЭ, проявляющейся как ТГВ и/или ТЭЛА. Наибольший риск развития ВТЭ наблюдается в первый год применения КОК; повышение риска развития этого осложнения наблюдается также при возобновлении применения КОК после перерыва в 4 недели и более. Некоторые эпидемиологические исследования показывают, что женщины, которые принимали низкодозированные КОК, содержащие 3 поколение прогестагенов, включая дезогестрел, имеют повышенный риск развития ВТЭ в сравнении с женщинами, принимающими низкодозированные КОК, содержащие в качестве прогестагена левоноргестрел, норгестимат или норэтистерон. Эти исследования продемонстрировали приблизительно 2-кратное увеличение риска развития ВТЭ. Частота развития ВТЭ в течение года у женщин, принимающих КОК, содержащие дезогестрел, составляет от 9 до 12 случаев на 10000 женщин; у женщин, не применяющих КОК, частота ВТЭ составляет 2 случая на 10000 женщин. Частота развития ВТЭ при применении КОК ниже, чем частота развития ВТЭ во время беременности (до 20 случаев на 10000 женщин) и послеродовом периоде (от 40 до 65 случаев на 10000 женщин).
ВТЭ может привести к летальному исходу в 1–2 % случаев.
Крайне редко на фоне приёма КОК тромбоз возникает в других кровеносных сосудах (например, в венах и артериях печени, брыжейки, почек, мозга или сетчатки глаза).
Симптомы ВТЭ и АТЭ: внезапная боль и/или отёк нижней конечности, внезапная интенсивная боль в груди, с иррадиацией в левую руку или без, внезапная одышка, внезапный кашель, необычная тяжёлая и длительная головная боль, внезапная частичная или полная потеря зрения, диплопия, нарушение речи или афазия, головокружение, коллапс с судорожным приступом или без него; слабость или выраженное онемение, внезапно появляющиеся на одной стороне тела, двигательные расстройства, «острый живот».
Риск развития ВТЭ возрастает при наличии следующих факторов риска:
- возраст;
- ожирение (ИМТ более 30 кг/м2);
- наличие в семейном анамнезе венозного или артериального тромбоза или тромбоэмболии у братьев, сестёр или родителей в возрасте менее 50 лет (если предполагается наличие наследственной предрасположенности — перед началом приёма КОК следует проконсультироваться со специалистом);
- длительная иммобилизация, серьёзное оперативное вмешательство, любая операция на нижних конечностях, в области таза, нейрохирургическое оперативное вмешательство или обширная травма. В этих случаях следует прекратить приём КОК (как минимум за 4 недели до планового хирургического вмешательства) и возобновить его только через 2 недели после полного восстановления мобильности женщины;
- временная иммобилизация, включая авиаперелёт длительностью более 4 часов, также является фактором развития ВТЭ особенно у женщин, имеющих другие факторы риска. Вопрос о возможной роли варикозного расширения вен и поверхностного тромбофлебита в развитии ВТЭ остаётся спорным.
Риск развития АТЭ возрастает при наличии следующих факторов риска:
- возраст;
- курение (риск увеличивается в большей степени у женщин старше 35 лет);
- дислипопротеинемия;
- ожирение (ИМТ более 30 кг/м2);
- артериальная гипертензия;
- мигрень;
- порок клапанов сердца;
- фибрилляция предсердий;
- наличие в семейном анамнезе венозного или артериального тромбоза, или тромбоэмболии у братьев, сестёр или родителей в возрасте менее 50 лет (если предполагается наличие наследственной предрасположенности перед началом приёма КОК следует проконсультироваться со специалистом).
Необходимо принимать во внимание повышение риска развития тромбоэмболии в послеродовом периоде.
Другие состояния/заболевания, при которых наблюдается нарушение кровообращения: сахарный диабет, системная красная волчанка, гемолитико-уремический синдром, хронические воспалительные заболевания кишечника (например, болезнь Крона или язвенный колит) и серповидно-клеточная анемия.
Увеличение частоты или интенсивности мигрени на фоне приёма КОК является основанием для немедленного прекращения его приёма (может быть продромальным синдромом нарушения мозгового кровообращения).
Биохимические факторы, которые могут указывать на наследственную или приобретённую предрасположенность к ВТЭ или АТЭ, включают резистентность к активированному протеину С, гипергомоцистеинемию, дефицит антитромбина III, дефицит протеина С, дефицит протеина S, антифосфолипидные антитела (антитела к кардиолипину, волчаночный антикоагулянт).
При оценке соотношения «польза/риск» применения КОК следует учитывать, что терапия данных состояний/заболеваний может снизить связанный с ними риск развития тромбоза или тромбоэмболии.
Опухоли
Наиболее важным фактором риска развития рака шейки матки (РШМ) является персистирующая папиломмавирусная инфекция (ВПЧ).
Эпидемиологические исследования показывают увеличение риска развития РШМ у женщин, инфицированных ВПЧ и длительно применяющих КОК (>5 лет), однако до настоящего времени существуют противоречия относительно степени влияния на эти данные различных факторов, в частности скрининговых обследований шейки матки или особенностей полового поведения женщины (количества половых партнёров и использование барьерных методов контрацепции), а также причинно-следственной взаимосвязи этих факторов.
По данным мета-анализа результатов 54 эпидемиологических исследований было выявлено небольшое повышение (в 1,24) риска развития рака молочной железы (РМЖ) у женщин, применяющих КОК. Повышенный риск постепенно уменьшается в течение 10 лет после отмены КОК. В связи с тем, что РМЖ отмечается редко у женщин до 40 лет, увеличение количества случаем РМЖ у женщин, принимающих КОК в настоящее время или принимавших его недавно, является незначительным по отношению к общему риску развития этого заболевания. Его связь с приёмом КОК не доказана. Наблюдаемое повышение риска может быть также следствием более ранней диагностики РМЖ у женщин, принимающих КОК (у них диагностируются более ранние клинические формы РМЖ, чем у женщин, не принимавших КОК), биологическим действием КОК или сочетанием обоих этих факторов.
Крайне редко при применении КОК наблюдались случаи развития доброкачественных, и ещё более редко — злокачественных опухолей печени.
В отдельных случаях такие опухоли приводили к представляющим угрозу для жизни женщины внутрибрюшному кровотечению, что следует учитывать при проведении дифференциального диагноза в случае появления сильных болей в области живота, увеличения печени или признаков внутрибрюшного кровотечения.
Другие состояния
Подавленное настроение и депрессия являются известной нежелательной реакцией при применении гормональных контрацептивов (см. раздел «Побочное действие»). Депрессия может быть серьёзным расстройством и является известным фактором риска суицидального поведения и суицида. Женщинам следует посоветовать обратиться к своему врачу в случае появления изменений настроения и депрессивных симптомов, в том числе, вскоре после начала приёма контрацептива.
У женщин с гипертриглицеридемией или соответствующим семейным анамнезом повышен риск развития панкреатита при приёме КОК.
У многих женщин принимающих КОК отмечалось небольшое повышение артериального давления (АД), клинически значимое повышение АД наблюдалось редко. Связь между приёмом КОК и артериальной гипертензией не установлена. Однако если на фоне приёма КОК развивается стойкое повышение АД, следует прекратить приём контрацептива и проводить антигипертензивную терапию. Приём КОК может быть продолжен, если на фоне гипотензивной терапии достигнуты нормальные значения АД.
На фоне беременности и во время приёма КОК наблюдалось развитие или ухудшение следующих состояний/заболеваний, хотя их взаимосвязь с приёмом КОК окончательно не установлена: желтуха и/или зуд, вызванные холестазом; образование камней в желчном пузыре, порфирия, системная красная волчанка, гемолитико-уремический синдром, хорея Сиденгама (малая хорея), гестационный герпес, потеря слуха вследствие отосклероза.
На фоне приёма КОК возможно ухудшение течения эндогенной депрессии, эпилепсии, болезни Крона и язвенного колита на фоне применения КОК.
У женщин с наследственными формами ангионевротического отёка экзогенные эстрогены могут вызывать или ухудшать симптомы ангионевротического отёка.
Острые или хронические нарушения функции печени могут служить основанием для отмены КОК до нормализации показателей функции печени. Рецидив холестатической желтухи, наблюдавшейся ранее во время предшествующей беременности или применения препаратов половых гормонов, требует отмены КОК.
Несмотря на то, что КОК могут оказывать влияние на инсулинорезистентность и толерантность к глюкозе, необходимость в коррекции дозы гипогликемических препаратов у пациенток с сахарным диабетом, принимающих низкодозированные КОК (<50 мкг этинилэстрадиола), как правило, отсутствует. Тем не менее, пациентки с сахарным диабетом должны находится под медицинским наблюдением и проводить регулярный контроль концентрации глюкозы в крови во время приёма контрацептива.
Иногда на фоне приёма КОК может развиваться хлоазма, особенно у женщин с наличием в анамнезе хлоазмы беременных. Женщины со склонностью к хлоазме во время приёма КОК должны избегать длительного прибывания на солнце и ультрафиолетового облучения.
Во время клинических исследований у пациенток с вирусным гепатитом С, получающими терапию лекарственными препаратами омбитасвира, паритапревира, ритонавира и дасабувира с рибавирином или без него, при одновременном приёме этинилэстрадиолсодержащих препаратов, таких как КОК, значительно чаще отмечалось увеличение концентрации печёночной трансаминазы АЛТ (в 5 раз выше верхней границы нормы). Женщины, принимающие препарат ПланиЖенс® дезо 30 должны перейти на альтернативный метод контрацепции (только прогестагенами или негормональными методами контрацепции). Приём препарата ПланиЖенс® дезо 30 должен быть прекращён до начала противовирусной терапии и может быть возобновлён не ранее чем через 2 недели после завершения терапии комбинацией противовирусных препаратов.
Медицинские осмотры/консулыпации
Необходимо ознакомиться с анамнезом жизни и семейным анамнезом женщины, провести тщательное общемедицинское (включая измерение АД, определение ИМТ) и гинекологическое обследование (с обязательным обследованием молочных желёз и цитологическим исследованием эпителия шейки матки), исключить беременность.
Объём дополнительных исследований и частота контрольных осмотров определяется индивидуально. Обычно контрольные обследования следует проводить не реже 1 раза в 6 месяцев.
Следует сообщить женщине, что препарат не предохраняет от ВИЧ-инфекции (СПИД) и других инфекций, передающихся половым путём!
Важно обратить внимание женщины на информацию о венозном и артериальном тромбозе/тромбоэмболии, в том числе, риске контрацепции препаратом ПланиЖенс® дезо 30 в сравнении с другими КОК, симптомах и известных факторах риска развития ВТЭ и АТЭ. Женщина должна получить рекомендации, что ей нужно делать в случае подозрения на тромбоз.
Снижение эффективности
Эффективность препарата ПланиЖенс® дезо 30 может снизиться в случае пропуска приёма таблеток, желудочно-кишечных расстройств или в результате лекарственного взаимодействия. Растительные препараты, содержащие зверобой продырявленный (Hypericum perforatum), не должны применяться на фоне приёма препарата ПланиЖенс® дезо 30 из-за риска снижения концентрации дезогестрела и этинилэстрадиола в плазме крови и, соответственно, контрацептивной эффективности препарата (см. разделы «Способ применения и дозы» и «Взаимодействие с другими лекарственными средствами»).
Недостаточный контроль цикла
На фоне приёма КОК могут отмечаться нерегулярные кровотечения («мажущие» кровянистые и/или «прорывные» кровотечения), особенно в течение первых месяцев применения. Поэтому оценка любых нерегулярных кровотечений должна проводиться только после периода адаптации, составляющего приблизительно 3 цикла приёма препарата.
Если нерегулярные кровотечения повторяются или развиваются после предшествующих регулярных циклов, следует провести тщательное обследование для исключения злокачественных новообразований или беременности.
У некоторых женщин во время перерыва в приёме таблеток может не развиться кровотечение «отмены». Если препарат ПланиЖенс® дезо 30 принимался согласно рекомендациям, беременность маловероятна. Тем не менее, если до этого контрацептив принимался нерегулярно или если отсутствуют подряд 2 кровотечения «отмены», до продолжения его приёма должна быть исключена беременность.
Лабораторные исследования
КОК могут влиять на результаты некоторых лабораторных исследований, включая биохимические показатели функции печени, щитовидной железы, надпочечников и почек, содержание транспортных белков в плазме, например, кортикостероид-связывающего глобулина (КСГ) и фракции липидов/липопротеинов, параметры углеводного обмена, коагуляции и фибринолиза. Обычно эти изменения находятся в пределах нормальных значений лабораторных показателей.
Влияние на способность управлять транспортными средствами или работать с механизмами
Приём препарата ПланиЖенс® дезо 30 не оказывает влияния на способность управлять транспортными средствами и механизмами.
Форма выпуска
Таблетки, 150 мкг + 30 мкг.
Хранение
Хранить в защищённом от света месте при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности.
Условия отпуска из аптек
Отпускают по рецепту
Классификация
-
Фармакотерапевтическая группа
-
АТХ
-
Действующее вещество
Подробнее по теме
Ознакомьтесь с дополнительными сведениями о препарате ПланиЖенс дезо 30:
